
Kelebihan Dan Kelemahan Teori Atom Thomson 2021 Riset
Video ini berisi penjelasan tentang cara menentukan konfigurasi elektron berdasarkan teori atom mekanika kuantum yang dilengkapi dengan contoh-contoh soal.RA.

KONFIGURASI ELEKTRON MENURUT TEORI ATOM BOHR & ELEKTRON VALENSI (KIMIA SMA KELAS 10) YouTube
Di dalam teori atas prinsip aufbau ini ada hal yang disebut dengan model kulit nuklir. Model yang satu ini dikenal sebagai suatu model yang digunakan untuk proses konfigurasi adanya proton dan neutron yang ada di dalam inti atom. Adanya prinsip aufbau ini dahulu dikemukakan oleh dua ilmuwan terkemukan yakni Niels Bohr dan Wolfgang Pauli.
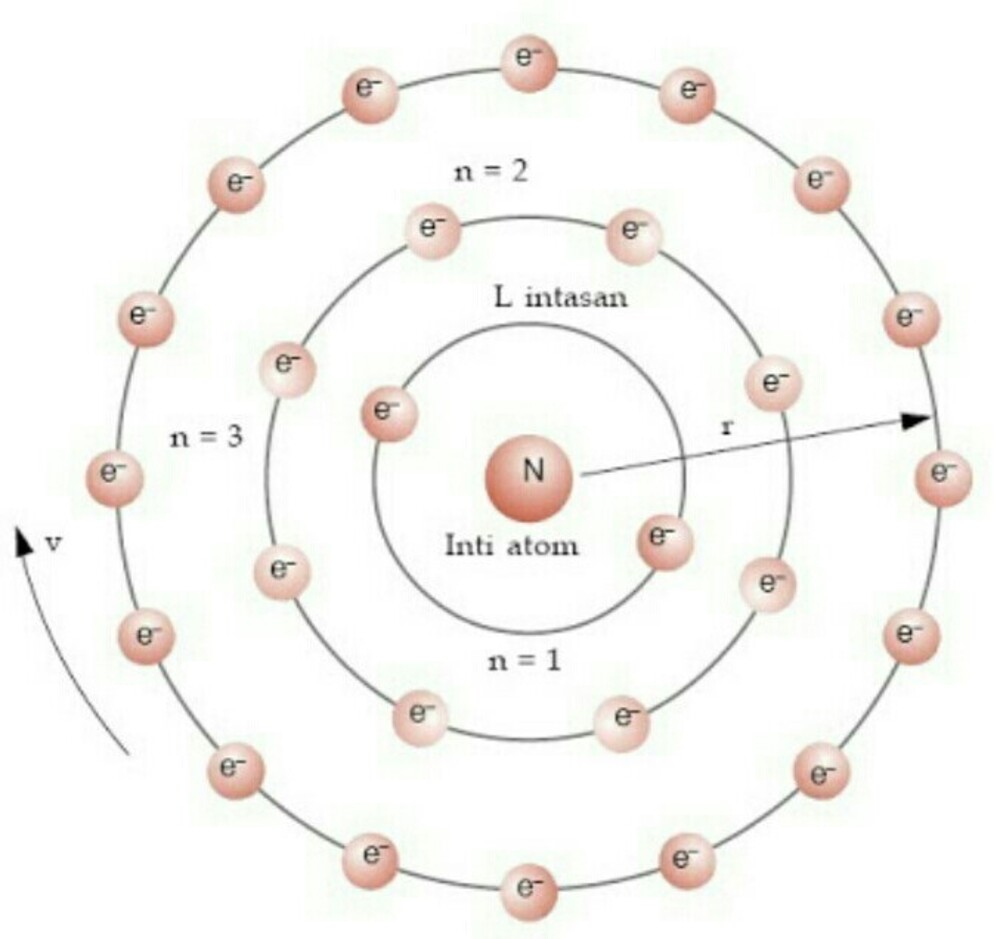
Mengenal Teori Atom Bohr dan Kekurangannya Nasional Katadata.co.id
About Press Copyright Contact us Creators Advertise Developers Terms Privacy Policy & Safety How YouTube works Test new features NFL Sunday Ticket Press Copyright.

Teori Struktur Keruangan Kota GeoHepi
Contoh Soal Konfigurasi Elektron akan membahas pengetahuan seputar mata pelajaran kimia yang berkaitan dengan atom. Dimana pada umumnya, konfigurasi elektron akan dikenalkan ataupun diajarkan pada siswa SMA kelas 10 atau sederajat. Berbicara seputar atom dari sudut pandang kimia, maka akan membahas mengenai tiga hal utama, yaitu inti atom.
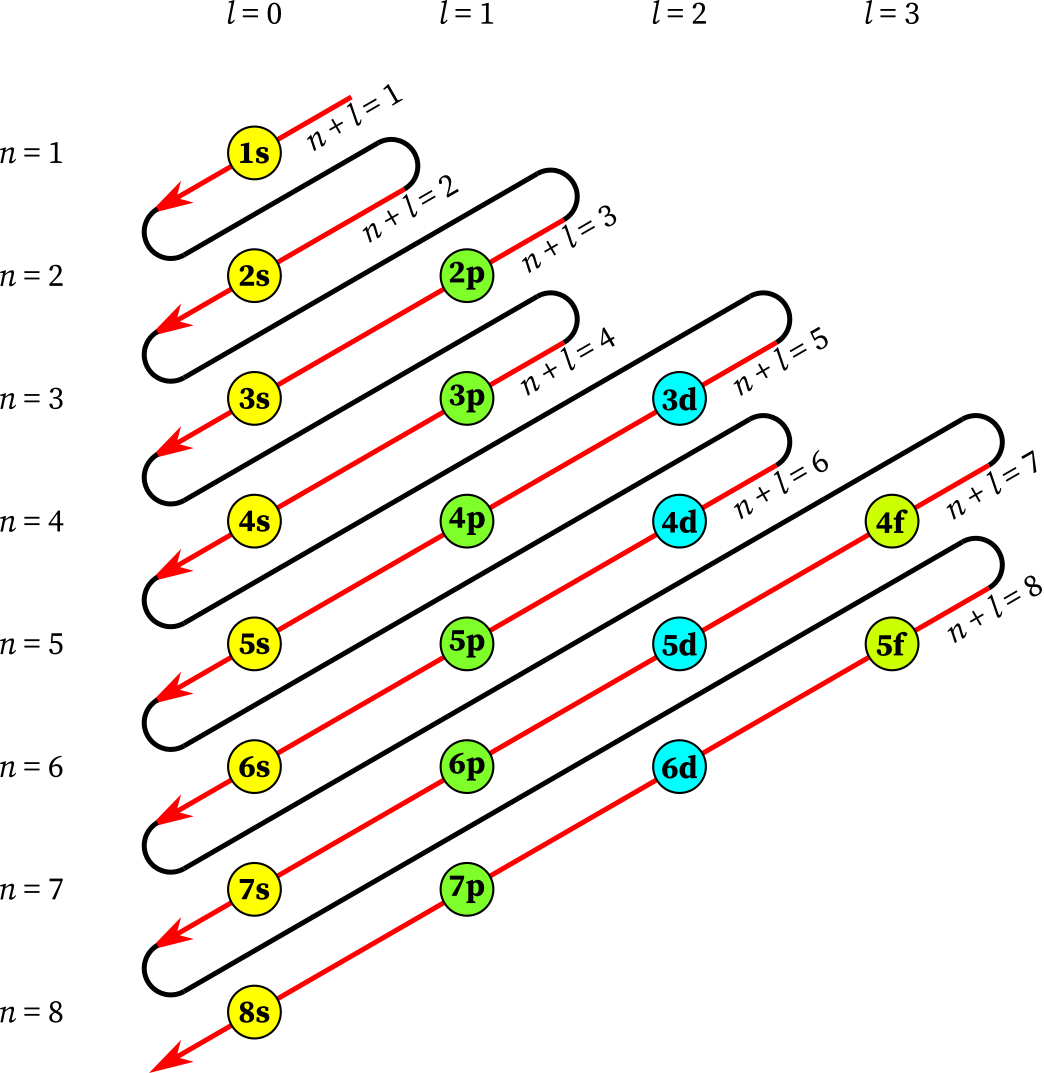
Diagrama de aufbau ¡Descarga & Ayuda 2021!
Teori aufbau menyajikan konfigurasi elektron dengan menggunakan bilangan kuantum dan aturan suksesi. Bilangan kuantum ini mengacu pada sifat-sifat partikel subatomik, seperti energi dan momentum, yang digunakan untuk memprediksi perilaku elektron dalam atom. Aturan suksesi, di sisi lain, mengikuti pola penempatan elektron yang berurutan sesuai.

Atomphysiker, Nobelpreisträger, Philosoph "Niels Bohr erfand die Wirklichkeit" ntv.de
KOMPAS.com - Model atom mekanika kuantum menyatakan bahwa elektron berada pada orbital-orbital atom.. Atom-atom tersebut menempati orbital sesuai dengan susunannya, atau yang disebut sebagai konfigurasi elektron.. Aturan dalam konfigurasi elektron terdiri dari tiga yakni Prinsip Aufbau, Aturan Hund, dan Larangan Pauli.. Prinsip Aufbau. Dilansir dari Encyclopaedia Britannica, Prinsip Aufbau.
Aufbau und Struktur Essay
Prinsip Aufbau menyatakan bahwa, secara hipotetis, elektron yang mengorbit satu atau lebih atom mengisi tingkat energi terendah yang tersedia sebelum mengisi tingkat yang lebih tinggi. Dengan cara ini, elektron pada atom, molekul, atau ion menyelaraskan ke konfigurasi elektron yang paling stabil.

XI.1.c. Aturan Aufbau (Teori) YouTube
2. Konfigurasi Elektron Berdasarkan Orbital (Teori atom Modern) Pengisian elektron berdasarkan orbital (teori atom modern) mengikuti beberapa aturan berikut. a. Asas Aufbau. Berdasarkan Asas Aufbau, pengisian orbital isi dasar bahwa elektron akan menempati kulit elektron dari subkulit yanbg tingkat energinya rendah ke tingkat yang energinya tinggi.
Ide Terpopuler Kerangka Teori
Model Atom Mekanika Kuantum. Model atom terakhir yang masih eksis hingga saat ini adalah mekanika kuantum. Model ini menyatakan bahwa atom terdiri dari inti atom yang bermuatan positif dan dikelilingi oleh awan-awan elektron. Dari teori inilah ditemukan empat jenis orbital, yaitu s, p, d, f. Berikut gambaran modelnya:

Struktur Atom (Kimia untuk SBMPTN) Asas Aufbau, Kaidah Hund, dan Asas Larangan Pauli YouTube
The Aufbau Principle (also called the building-up principle or the Aufbau rule) states that, in the ground state of an atom or ion, electrons fill atomic orbitals of the lowest available energy level before occupying higher-energy levels. In general, an electron will occupy an atomic orbital with the lowest value of n, l,ml n, l, m l, in that.

Aufbau Principle — Overview & Application Expii
Nah sekarang kita akan menggambarkan konfigurasi elektron memakai diagram orbital, teman. Sebenarnya gambarnya cukup mudah kok. Suatu subkulit punya sejumlah orbital. Orbital itu digambarkan sebagai persegi dan berisi garis setengah panah yang mewakili elektron. Subkulit s punya 1 orbital, p punya 3 orbital, d punya 5 orbital, dan f 14 orbital.
PPT A. Perkembangan Teori atom PowerPoint Presentation, free download ID4194153
The Aufbau Process is all about keeping electrons at their lowest possible energy and is the direct result of the Pauli Exclusion Principle. A corollary of Coulomb's law is that the energy of an electron is affected by attractive and repulsive forces. The closer an electron is to the nucleus, the lower its energy.

Jelaskan Bagaimana Bunyi Postulat Bohr Dalam Menjelaskan Teorinya Tugas sekolah
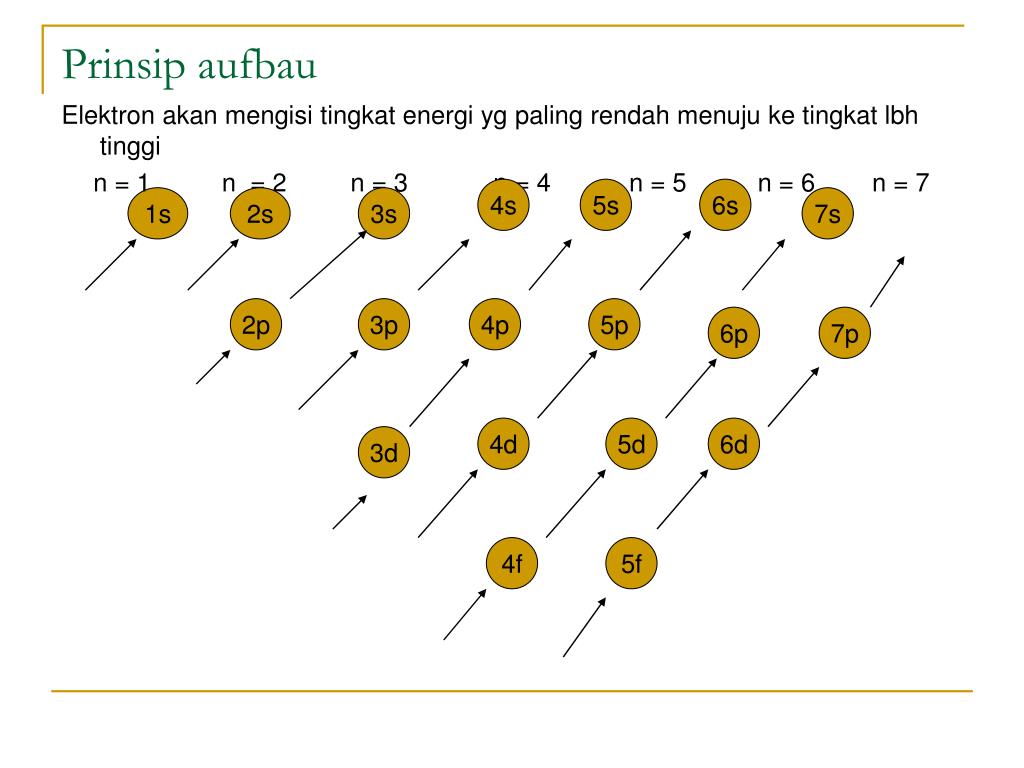
Prinsip Aufbau: Elektron menempati orbital-orbital dimulai dari tingkat energi yang terendah, dimulai dari 1s, 2s, 2p, dan seterusnya seperti urutan subkulit yang terlihat pada Gambar. Gambar 2. Prinsip Aufbau. Ada 4 subkulit yaitu: s, p, d, dan f dan angka sebelum subkulit menunjukkan kulit. Sub kulit 1s punya tingkat energi paling rendah.

SOLUTION Teori aufbau Studypool
Konfigurasi elektron adalah suatu cara penulisan yang menunjukkan distribusi elektron dalam orbital-orbital pada kulit utama dan subkulit. Pada penulisan konfigurasi elektron perlu mempertimbangkan tiga aturan yaitu prinsip Aufbau, asas larangan Pauli dan kaidah Hund. Prinsip Aufbau Elektron-elektron dalam suatu atom berusaha menempati subkulit-subkulit yang berenergi rendah, kemudian baru ke.

TEORI ATOM MODERN DAN KONFIGURASI ELEKTRON AUFBAU YouTube
Pengertian Prinsip Aufbau. Prinsip Aufbau didasarkan pada teori konfigurasi elektron yang menyatakan bahwa ketika elektron dimasukkan ke dalam inti atom, hal yang sama akan terjadi dengan elektron sehingga keseimbangan muatan unsur dapat dipertahankan. Dengan cara ini, aturan tertentu ditetapkan untuk dapat menempatkan mereka di orbital atom.

Download Contoh Soal Konfigurasi Elektron Aufbau + Jawaban Dikdasmen
Sejarah Prinsip Aufbau dalam teori kuantum baru Dalam teori kuantum lama, orbit dengan momentum sudut rendah (s- dan p- orbital) lebih dekat ke inti.. Prinsip ini mengambil namanya dari Jerman, Aufbauprinzip, "prinsip membangun", bukannya diberi nama seorang ilmuwan.Bahkan, ia dirumuskan oleh Niels Bohr dan Wolfgang Pauli di awal 1920-an, dan menyatakan bahwa: