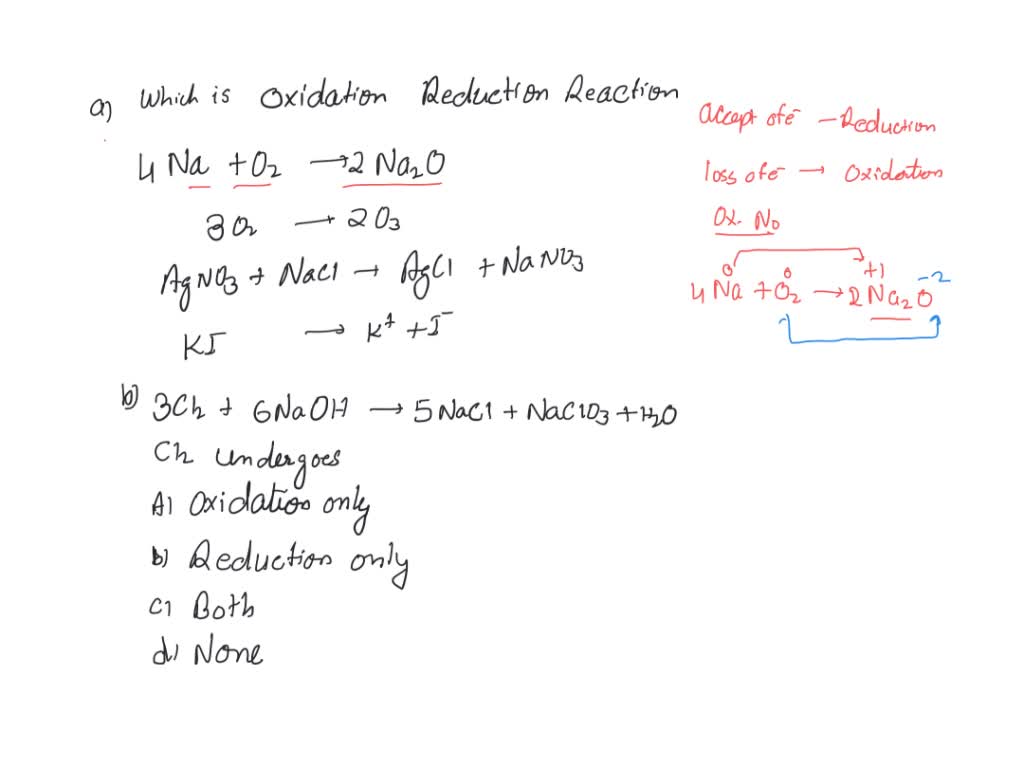
SOLVED termaksud reaksi reduksi atau oksidasikah perubahan berikut so23>SO42 Fai Ld Termasuk
Pereduksi atau reduktor adalah zat yang dapat menyebabkan zat lain mengalami reaksi reduksi (pereduksinya sendiri mengalami reaksi oksidasi).Pengoksidasi atau oksidator adalah suatu zat yang dapat menyebabkan zat lain mengalami reaksi oksidasi (pengoksidasi mengalami reaksi reduksi). Reduktor dan oksidator dapat ditentukan dengan terlebih dahulu mengetahui biloks unsur yang berubah sebagai.

Perhatikan persamaan reaksi berikut! CH4(g) + O2(g) → CO2(g) + H2O(l) a. Tentukan zat pereaksi
Oke, kita lanjut ya bahasannya! Pada reaksi redoks, terdapat unsur-unsur yang bertindak sebagai reduktor dan oksidator. Zat yang mengalami oksidasi itu disebut reduktor, sedangkan zat yang mengalami reduksi disebut oksidator. Coba perhatikan contoh berikut ini, ya! Reaksi: Mg(s) + 2HCl -----> MgCl2(aq) + H2(g) Karena Mg merupakan unsur bebas, jadi biloks Mg = 0.

Tentukan bilangan oksidasi, jenis reaksi dan sifat zat (z...
Reduktor dan Oksidator Artikel Reduktor dan Oksidator ini berisi uraian tentang pengoksidasi (oksidator) dan zat pereduksi (reduktor). Untuk reaksi-reaksi tersebut lihat: Redoks (Reduksi dan Oksidasi) Kimia Beserta Contoh Soal dan Jawaban Oksidator Dalam kimia, zat pengoksidasi, dalam bahasa Indonesia lebih dikenal sebagai oksidator, memiliki 2 makna.

Zat yang berperan sebagai pereduksi ? Reaksi Redoks Reduktor YouTube
Z at pengoksidasi adalah NiO, sedangkan zat pereduksi adalah H2. Pereduksi atau reduktor adalah zat yang dapat menyebabkan zat lain mengalami reaksi reduksi (pereduksinya sendiri mengalami reaksi oksidasi). Pengoksidasi atau oksidator adalah suatu zat yang dapat menyebabkan zat lain mengalami reaksi oksidasi (pengoksidasi mengalami reaksi reduksi).

tentukan zat pengoksidasi dan pereduksi dari zat kimia berikut(lihat gambar)yang lengkap dan
Berikut beberapa contohnya. Baca juga: Contoh soal hukum Faraday 1 dan 2. Pengoksidasi dan Pereduksi. Didalam reaksi redoks atau reaksi reduksi oksidasi, terdapat agen pereduksi dan agen pengoksidasi. Pereduksi disebut juga reduktor, merupakan zat yang terlibat di dalam reaksi redoks yang menyebabkan zat lain mengalami reduksi.
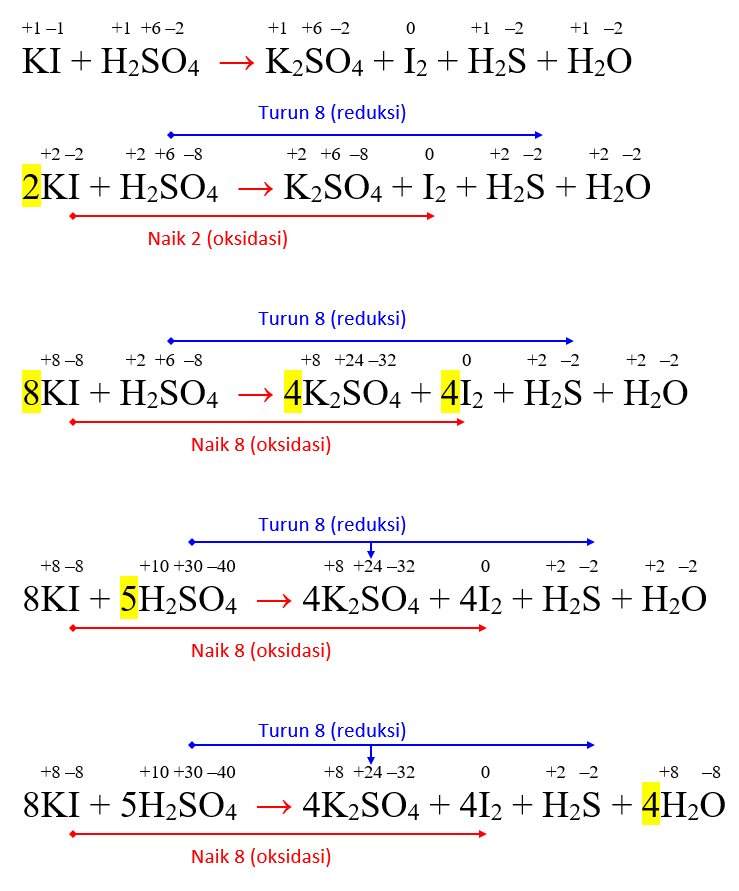
Penyetaraan Reaksi Redoks KI + H2SO4 → K2SO4 + I2 + H2S + H2O Serba Ada
Kimia; Kimia Fisik dan Analisis Kelas 10 SMA; Reaksi Reduksi dan Oksidasi serta Tata Nama Senyawa; Konsep Reaksi Reduksi dan Oksidasi; Tentukan zat pengoksidasi dan zat pereduksi dari persamaan kimia berikut a. CH4 + 2O2 -> CO2 + 2H2O b. 2Ca + O2 -> 2CaO. Konsep Reaksi Reduksi dan Oksidasi; Reaksi Reduksi dan Oksidasi serta Tata Nama Senyawa

PPT 1). Cara setengah reaksi setiap persamaan reaksi redoks merupakan penjumlahan 2 setengah
Pembahasan. Zat pengoksidasi adalah O2, sedangkan zat pereduksi adalah atom Ca. Pereduksi atau reduktor adalah zat yang dapat menyebabkan zat lain mengalami reaksi reduksi (pereduksinya sendiri mengalami reaksi oksidasi). Pengoksidasi atau oksidator adalah suatu zat yang dapat menyebabkan zat lain mengalami reaksi oksidasi (pengoksidasi.

Menyetarakan Reaksi Redoks dengan cara setengah reaksi YouTube
Karena zat pereduksi selalu diubah menjadi zat pengoksidasi konjugatnya dalam reaksi reduksi oksidasi, produk dari reaksi ini termasuk zat pengoksidasi baru (Al2O3) dan zat pereduksi baru (Fe). Karena reaksi berlangsung ke arah ini, tampaknya masuk akal untuk mengasumsikan bahwa bahan awal mengandung zat pereduksi yang lebih kuat dan zat.

Contoh Soal Persamaan Reaksi Kimia Homecare24
Pengertian pengolahan limbah adalah proses penghilangan kontaminan dari air limbah industri dan limbah rumah tangga, untuk menghindari polusi pada lingkungan. Konsep Redoks. Ada beberapa definisi reaksi redoks (reaksi oksidasi dan reduksi) beserta contoh reaksi oksidasi dan reduksi, sebagai berikut. 1. Berdasarkan penangkapan atau pelepasan oksigen

Persamaan Laju Reaksi Penjelasan, Rumus, Contoh Soal dan Jawaban
Susunlah unsur A, B, C, dan D berdasarkan daya pereduksinya dari paling kuat! Pembahasan Contoh Soal 2: Dimisalkan E o oks A= 0 (sekadar sebagai acuan) Dari reaksi (1) urip.info E o sel = E o oks A + E o red B +0,38 Volt = 0 + E o red B E o red B = +0,38 Volt E o oks B = -0,38 Volt Dari reaksi (2) urip.info E o sel = E o oks B + E o red D +1.
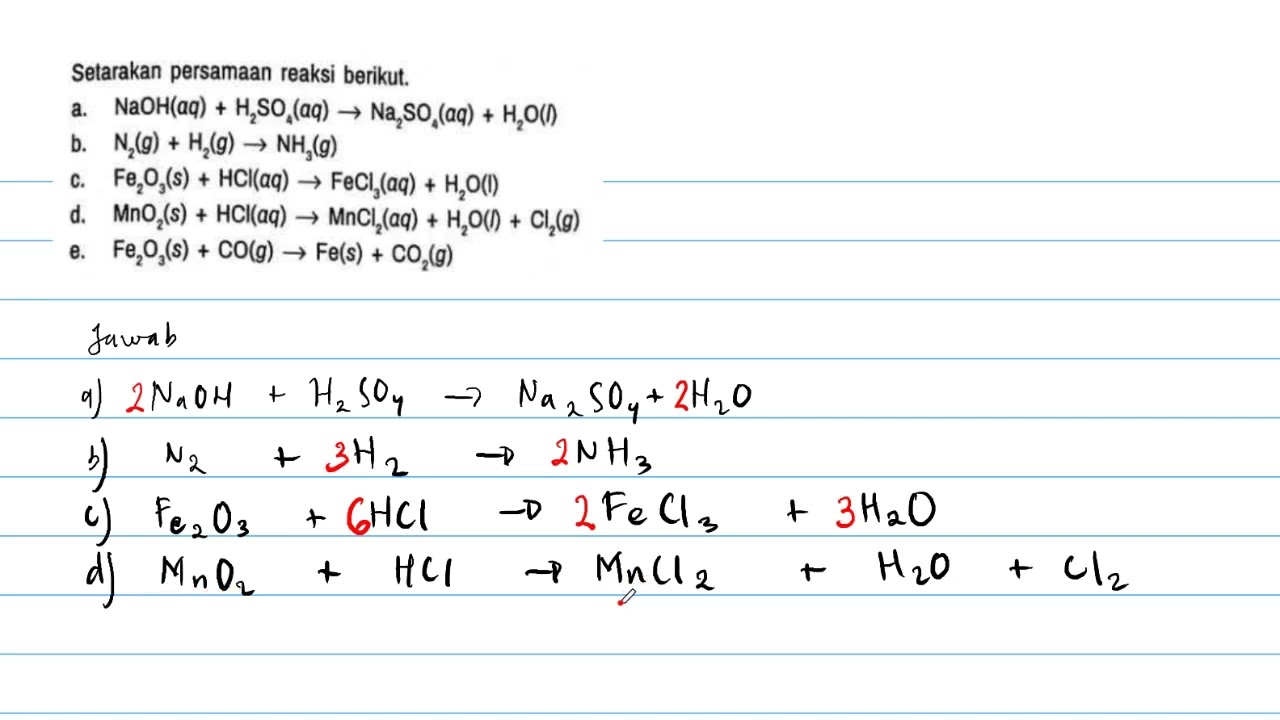
Setarakan persamaan reaksi berikut YouTube
Berikut ini contoh dan jenis-jenis reaksi reduksi oksidasi, di antaranya: 1. Reaksi Kombinasi. Reaksi kombinasi adalah jenis reaksi redoks yang paling sederhana, yang melibatkan penggabungan elemen menjadi suatu senyawa kimia. Dalam reaksi redoks, baik reduksi maupun oksidasi terjadi pada saat yang sama.

Tentukan zat yang mengalami oksidasi dan reduksi dari persamaan reaksi dibawah ini C2H6 + O2
Reaksi oksidasi adalah proses kimia di mana suatu zat kehilangan elektron atau menambahkan oksigen. Ini adalah salah satu jenis reaksi redoks (oksidasi reduksi), yang melibatkan transfer elektron antara zat-zat kimia. Untuk memahami lebih lanjut, mari kita bahas unsur-unsur kunci yang terlibat dalam reaksi oksidasi.

Contoh Soal Reaksi Asam Basa Konjugasi Kumpulan Contoh Soal My XXX Hot Girl
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Tentukan zat pengoksidas.

Cikgu Nurul Asas Kimia Membina Persamaan Kimia Seimbang
Berikut pengertian dari kedua istilah tersebut. 1. Pengertian Reduksi. Reduksi adalah reaksi penangkapan elektron atau reaksi penurunan bilangan oksidasi, sedangkan reduktor merupakan zat yang melakukan proses reduksi terhadap zat lainnya. Reduksi merupakan peristiwa reaksi yang mengalami penurunan bilangan oksidasi dan kenaikan elektron.

Perubahan Entalpi Pembakaran Standar Adalah Penggambar
Zat pengoksidasi adalah O2, sedangkan zat pereduksi adalah C2H4. Pereduksi atau reduktor adalah zat yang dapat menyebabkan zat lain mengalami reaksi reduksi (pereduksinya sendiri mengalami reaksi oksidasi). Pengoksidasi atau oksidator adalah suatu zat yang dapat menyebabkan zat lain mengalami reaksi oksidasi (pengoksidasi mengalami reaksi reduksi).
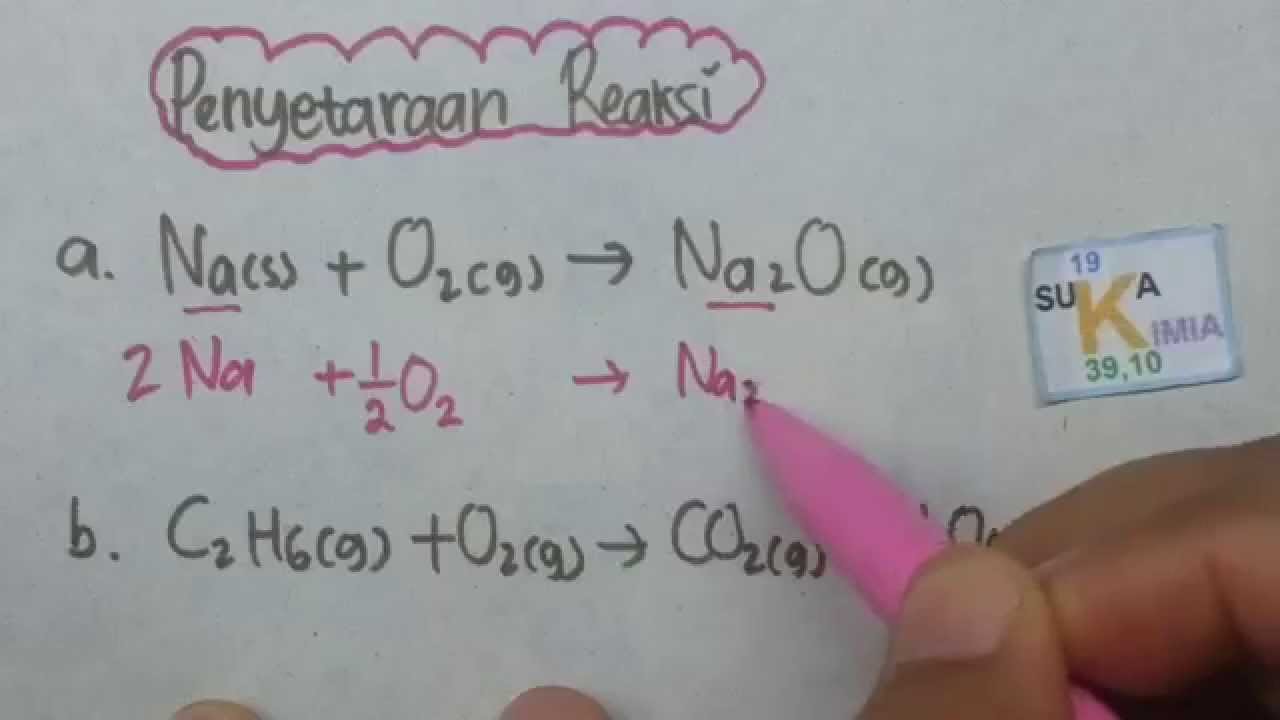
Contoh Soal Persamaan Reaksi Kimia Dan Jawabannya Contoh Soal Terbaru
Tentukan oksidator, reduktor, hasil oksidasi dan hasil reduksi pada reaksi redok berikut. MnO 2 + 4HCl → MnCl 2 + Cl 2 + 2H 2 O. PEMBAHASAN : MnO 2 mengalami penurunan biloks sehingga mengalami reaksi reduksi atau sebagai OKSIDATOR. HCl mengalami kenaikan biloks sehingga mengalami reaksi oksidasi atau sebagai REDUKTOR.