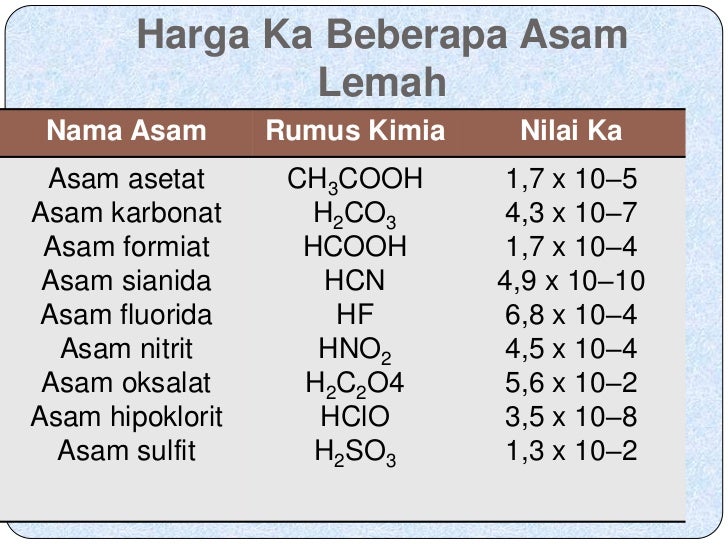
Nama Asam Dan Basa Beserta Rumus Kimianya
With an old townhouse feel just a five-minute walk from Teatro alla Scala, the Grand Hotel et de Milan has opera ties and old-world glamour that make the experience unrepeatable in any other city.

LENGKAP ‼️ Cara Mudah Menentukan Pasangan Asam Basa Konjugasi TeoriAsamBasa AsamBasaKonjugasi
Senyawa poliatomik dari kation monoatomik dan anion poliatomik. Senyawa poliatomik terdiri dari kation monoatomik dan anion poliatomik yaitu dengan menuliskan terlebih dahulu nama ion monoatomik lalu disusul dengan nama ion poliatomik, seperti contoh berikut ini. # Kation monoatik seperti natrium Na +, magnesium Mg 2+, dan aluminium Al 3+.
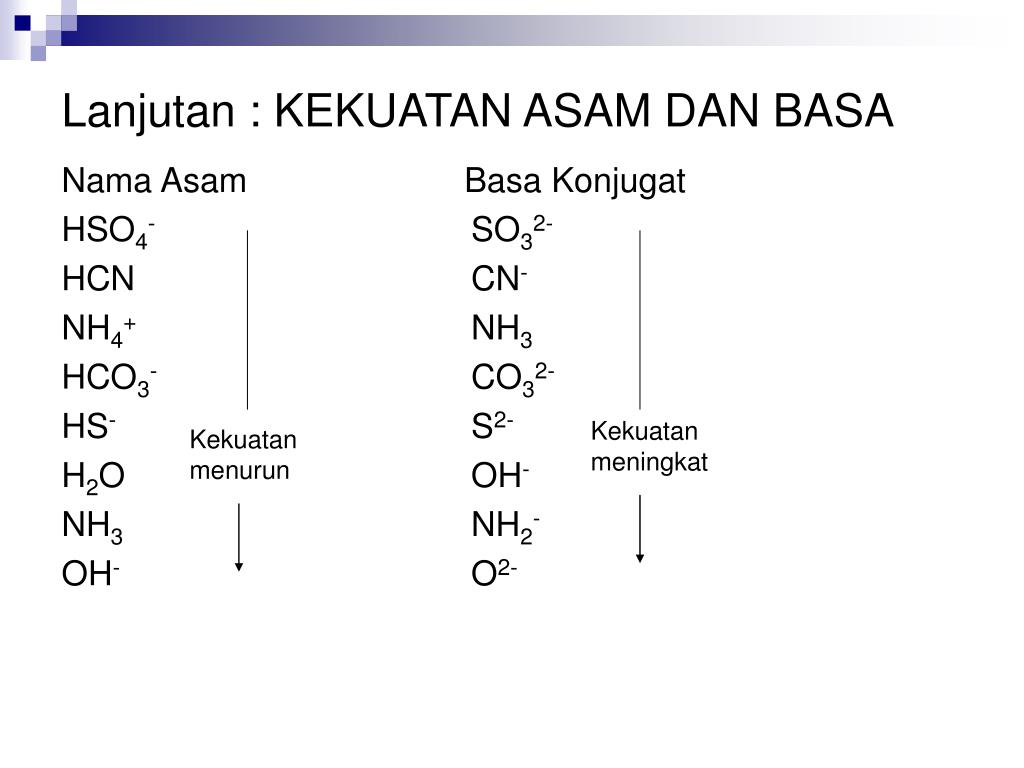
PPT ASAM DAN BASA PowerPoint Presentation, free download ID4714427
Video ini berisi materi tata nama senyawa poliatomik, seanyawa asam dan basa. Materi dilengkapi dengan coontoh soal yang akan mempermudah dalam memahami maer.

15+ Contoh Soal Tata Nama Senyawa Asam Dan Basa Contoh Soal Terbaru
Berikut ini contoh asam dan basa yang ada di sekitarmu: Asam. Jeruk yang mengandung C 6 H 8 O 7. Cuka yang mengandung CH 3 COOH. Sengat lebah yang mengandung HCOOH. Aki Mobil yang mengandung H 2 SO 4. Basa. Sabun yang mengandung NaOH; Cara membedakan asam dan basa. Cara membedakan asam dan basa tidaklah sulit. Kamu bisa melihat dari ciri-ciri.

Daftar Senyawa Asam Dan Basa
Asam dan basa bersifat saling menetralkan. Jadi bila kedua zat ini dicampurkan, maka sifat asal dari masing-masing zat dapat hilang. Nama asam (acid) berasal dari bahasa Latin 'acetum' yang artinya adalah 'cuka'.. Tata Nama Senyawa Asam-Basa menurut IUPAC, Materi Kimia Kelas 10. Contoh Soal Asam Basa dan Jawaban, Materi IPA Kelas 7.
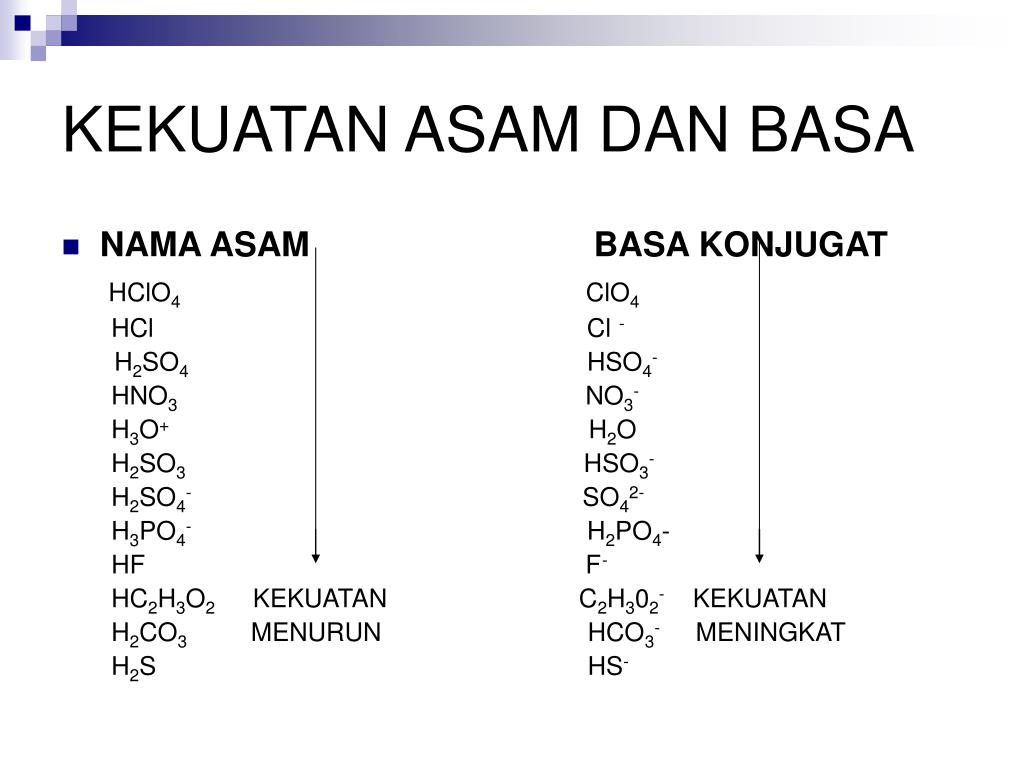
PPT ASAM DAN BASA PowerPoint Presentation, free download ID1244635
Pengertian Asam, Basa, dan Garam. Asam. Svante August Arrhenius, seorang ahli kimia asal Swedia yang hidup tahun 1859-1927 menjabarkan pengertian asam sebagai: semua zat atau senyawa elektrolit yang jika dilarutkan dalam air akan terurai menghasilkan ion H+ (hidrogen) dan ion sisa asam yang bermuatan negatif, demikian menurut Modul Guru.
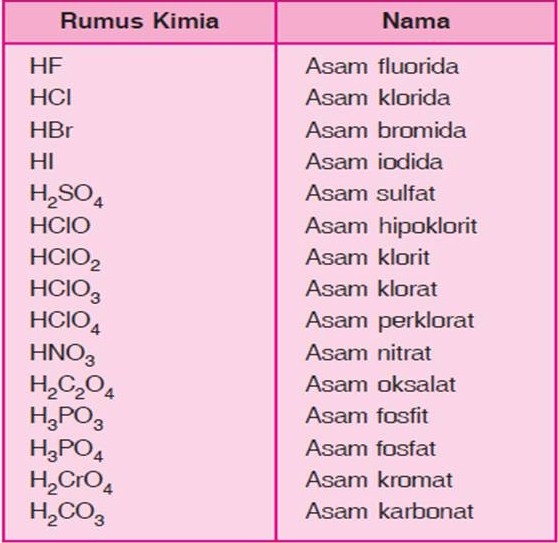
Nama Senyawa Hbr
Materi pelajaran Kimia untuk SMA Kelas 11 IPA bab Teori dan Karakteristik Asam-Basa ⚡️ dengan Karakteristik dan Tata Nama Asam dan Basa, bikin belajar mu makin seru dengan video belajar beraminasi dari Ruangbelajar.. Video ini membahas soal tata nama senyawa asam. Karakteristik Senyawa Basa. Video ini membahas tentang karakteristik.

15+ Contoh Soal Tata Nama Senyawa Asam Dan Basa Contoh Soal Terbaru
Akan tetapi, asam merupakan senyawa molekul bukan senyawa ion. Penamaan senyawa asam dilakukan dengan menambahkan kata asam di depan lalu diikuti dengan anion sebagai sisa asam. HA -> H+ + A-. Sedangkan basa merupakan larutan yang menghasilkan ion OH - dan sisa basanya berupa logam (golongan IA, IIA, Al dan Fe).

Cara Menentukan Senyawa Bersifat Asam Basa Atau Netral Digunakan
Belajar larutan asam basa dengan video dan kuis interaktif di Wardaya College. Dapatkan pelajaran, soal. dan rumus larutan asam basa lengkap SMA.. Kamu akan dijelaskan mengenai konsep oksida, jenis-jenis oksida, bahkan tata nama senyawa oksida dengan rinci dan mendetil. Selanjutnya, kamu bisa mengakses contoh soal larutan asam basa yang.

TATA NAMA SENYAWA ASAM, BASA, DAN GARAM YouTube
Pada umumnya senyawa ini dibentuk oleh ion-ion poliatomik. a. Anion poliatomik umumnya lebih banyak dibandingkan kation poliatomik. Suatu kation poliatomik yang umum dijumpai adalah NH4+. b. Hanya sedikit anion poliatomik yang memiliki nama dengan akhiran "ida". Hanya OH- (ion hidroksida) dan CN- (ion sianida).

15+ Contoh Soal Tata Nama Senyawa Asam Dan Basa Contoh Soal Terbaru
Garam merupakan senyawa hasil reaksi antara asam dengan basa, misalnya garam CuSO 4.Garam terdiri dari kation dari basa dan anion dari asam. Penamaan garam sama dengan tata nama senyawa ion yaitu dengan menyebut nama kation diikuti nama anionnya. Khusus kation dari unsur yang memiliki bilangan oksidasi lebih dari satu (ex. Sn, Pb, Fe, Cu dan Au) bilangan oksidasinya ditulis dalam kurung dengan.

Tata Nama Senyawa Asam dan Basa Gulai Schoolstudies MA Pembangunan YouTube
Berikut adalah beberapa contoh tata nama asam: H 2 SO 4: Asam Sulfat; HNO 3: Asam Nitrat; Tata nama basa adalah pemberian nama senyawa yang terbentuk akibat senyawa berikatan dengan anion OH-. Untuk aturan di dalam pemberian nama basa adalah sebagai berikut: Basa mempunyai anion OH- di dalam senyawanya sehingga akan ditulis pada bagian belakang.

Tata Nama Senyawa Ion, Poliatom, Asam dan Basa YouTube
Tata nama senyawa asam dan basa diperlakukan untuk memberikan nama pada senyawa-senyawa asam dan basa sehingga lebih mudah untuk diidentifikasi dan dikelompokkan. 1. Tata Nama Senyawa Asam Aturan tata nama senyawa asam adalah sebagai berikut: Memberikan awalan asam (hidro) Diikuti dengan nama pasangannya Diakhiri dengan akhiran -ida. Tetapi ada beberapa senyawa asam yang tidak memiliki akhiran.

Tata Nama Senyawa Poliatomik, Asam, dan Basa Kimia Kelas 10 YouTube
Tata nama senyawa kovalen. b. Tata nama senyawa ion. c. Tata nama senyawa asam. d. Tata nama senyawa basa. e. Tata nama senyawa garam. Dalam bahasan kali ini, kita akan mendalami tatanama senyawa asam, basa, dan garam, sebagaimana disarikan dari Modul Pembelajaran Kimia SMA Kelas 10 yang diitulis oleh Wiwik Indah Kusumaningrum, S.Pd., M.Pd.
15+ Contoh Soal Tata Nama Senyawa Asam Dan Basa Contoh Soal Terbaru
Berdasarkan definisi asam basa oleh Arrhenius, senyawa asam adalah senyawa yang bila dilarutkan dalam air akan melepas ion H +. Pada umumnya, asam dapat terionisasi dalam air menjadi ion H + dan anion yang disebut sisa asam. Penamaan senyawa asam dimulai dari kata 'asam' diikuti dengan nama anion sisa asam. Contoh: HCl : asam klorida

Tata Nama Senyawa dan Persamaan Reaksi Sederhana
Penulisan tata nama senyawa anorganik berikutnya adalah senyawa asam dan basa. Berikut penulisan tata nama senyawanya. Senyawa asam. Arrhenius mendefinisikan senyawa asam sebagai senyawa yang apabila dilarutkan dalam air akan menghasilkan ion H+. Penulisan tata nama senyawa ini dimulai dengan menuliskan unsur asam terlebih dahulu, lalu diikuti.