
(DOCX) RPP Kesetimbangan Kimia 1 (Kesetimbangan Dinamis) DOKUMEN.TIPS
Di mana prinsip ini digunakan untuk memanipulasi reaksi reversibel dan meningkatkan rendemen reaksi. Kurang lebih begitulah pembahasan mengenai materi kesetimbangan kimia kelas 11. Semoga setelah membaca artikel ini Sobat Zenius jadi semakin paham, ya dan nggak kesulitan lagi saat mengerjakan soal tentang materi yang satu ini.

Kesetimbangan Kimia 1 Kesetimbangan Dinamis YouTube
Suatu reaksi kesetimbangan bersifat dinamis dan berlangsung dalam sistem tertutup.. ↔ 2NH3(g) CaCO3(s) ↔ CaO(s) + CO2(g) 2. Bersifat dinamis: Artinya secara makroskopis reaksi berlangsung terus menerus dalam dua arah dengan laju yang sama, dapat dilihat dari perubahan suhu , tekanan, konsentrasi atau warnanya .. Kesetimbangan dalam.

PPT Kesetimbangan Kimia PowerPoint Presentation, free download ID6442863
Reaksi kesetimbangan kesetimbangan bersifat dinamis mikroskopis artinya terjadi pergerakan molekul molekul secara berkelanjutan dan terus menerus. Sedangkan. Demikian jawaban dari pertanyaan Suatu sistem kesetimbangan bersifat dinamis mikroskopis, berarti?, Semoga bisa membantu kamu ya teman. Jika kamu masih punya pertanyaan lainnya, bisa.
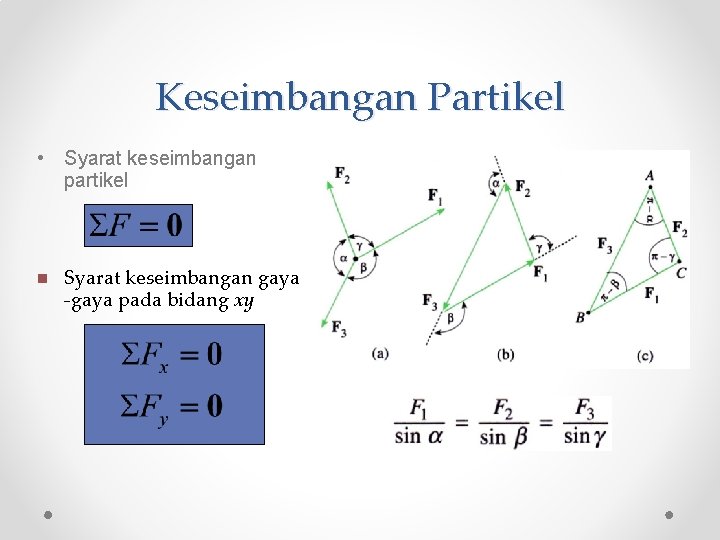
Contoh Soal Kesetimbangan Partikel Kesetimbangan Kimia Dinamis Images and Photos finder
Andi M. 05 Maret 2022 07:19. Suatu sistem kesetimbangan bersifat dinamis-mikroskopis, artinya . A. perubahan berlangsung terus-menerus dan dapat diamati B. reaksi terus berlangsung ke kanan dan ke kiri dan dapat diamati C. reaksi terus berlangsung ke kanan dan ke kiri tetapi tidak teramati D. perubahan berlangsung terus berhenti sehingga tidak.

Pengertian Kesetimbangan Kimia Konsep Dasar, Faktor dan Contoh Soal Gramedia Literasi
kesetimbangan dinamis, artinya reaksi ke kanan maupun ke kiri terus berlangsung tetapi dengan kecepatan yang sama. Contoh Kesetimbangan dinamis Reaksi: N 2O 4 (g) = 2NO 2 (g) Untuk membuktikan bahwa kesetimbangan adalah dinamis, dilakukan percobaan reaksi antara ion besi (III) dengan ion tiosianat SCN−: Fe(H 2O) 6

Kesetimbangan Kimia Part 1 kesetimbangan Dinamis YouTube
Contoh 1. Pada reaksi kesetimbangan peruraian gas N2O4 menjadi gas NO2, tercapai keadaan setimbang saat kecepatan terurainya N2O4 sama besarnya dengan kecepatan membentuk kembali N2O4. N2O4 (g) ⇄ 2 NO2 (g) Tercapainya kesetimbangan dinamis peruraian N2O4 dapat dilihat pada gambar berikut: (a) Reaksi dimulai, campuran reaksi terdiri dari N2O4.

Kesetimbangan Dinamis YouTube
Latihan Soal Kesetimbangan Kimia (Sukar) Pertanyaan ke 1 dari 5. Pada suhu 300 K ke dalam wadah bervolume 2 L dimasukkan 0,1 mol N2 dan 0,1 mol Cl2 berdasarkan reaksi berikut: H2(g)+Cl2(g)⇌ 2HCl(g) Jika harga tetapan kesetimbangan KC = 16. Maka jumlah mol dari gas HCl yang diperoleh adalah. . 0,07 mol.

Sistem kesetimbangan dinamis mikroskopis adalah suatu kea...
Ini adalah contoh kesetimbangan dinamis. Kesetimbangan, seperti sisa termodinamika, adalah fenomena statistik, rata-rata perilaku mikroskopis. Prinsip Le Châtelier (1884) memberi gambaran tentang perilaku suatu sistem kesetimbangan saat perubahan kondisi reaksinya terjadi.

Perhatikan gambar di bawah ! Suatu sistem kesetimbangan y...
Suatu sistem kesetimbangan bersifat dinamis-mikroskopis berarti…. A. Perubahan berlangsung terus-menerus dan dapat diamati B. Reaksi terus berlangsung kekanan dan kekiri dan dapat diamati C. Reaksi terus berlangsung kekanan dan kekiri tetapi tidak teramati D. Perubahan berlangsung terus berhenti sehingga tidak dapat diukur

KESETIMBANGAN DINAMIS YouTube
Sistem kesetimbangan dinamis mikroskopis adalah su. Sistem kesetimbangan dinamis mikroskopis adalah suatu keadaan yang menyatakan. reaksi terus berlangsung ke kanan dan ke kiri serta tidak dapat diamati. zat hasil reaksi tidak bereaksi karena telah mencapai keadaan setimbang. reaksi berlangsung terus-menerus dalam satu arah dan tidak dapat.

Sistem kesetimbangan dinamis mikroskopis adalah suatu kea...
Kesetimbangan tercapai pada saat laju reaksi pembentukan produk sama dengan laju reaksi pembentukan reaktan. Pada keadaan setimbang tidak terjadi perubahan makroskopis, tetapi pada tingkat mikroskopis reaksi tetap berlangsung. Oleh karena itu, kesetimbangan kimia disebut juga kesetimbangan dinamis. Jadi, jawaban yang tepat adalah C.

A. Konsep Kesetimbangan Dinamis 1. Reaksi Kimia Reversible Dan Irreversible PDF
kesetimbangan. Keadaan seperti ini dikatakan bahwa kesetimbangan bersifat dinamis. Keadaan dinamis hanya terjadi dalam sistem tertutup. Contoh kesetimbangan dinamis dalam kehidupan sehari-hari yaitu proses pemanasan air dalam wadah tertutup. Saat suhu mencapai 100°C air akan berubah menjadi uap dan tertahan oleh tutup.

PPT Kesetimbangan Kimia PowerPoint Presentation, free download ID6442863
Untuk informasi lebih jelas mengenai kesetimbangan kimia, mulai dari pengertian, jenis, rumus, hingga contoh soalnya, kamu bisa menyimaknya dalam ulasan berikut ini, ya! 1. Pengaruh volume terhadap kesetimbangan. 2. Pengaruh tekanan terhadap kesetimbangan. 3. Pengaruh suhu terhadap kesetimbangan. 4.

Contoh Soal Kesetimbangan Dinamis Beserta Penjelasannya
Reaksi Kimia dalam Konsep Kesetimbangan. Dikutip dari Modul Paket Keahlian Kimia Kesehatan SMK (2016), dalam konsep kesetimbangan, reaksi kimia berdasarkan sifat berlangsungnya, dibedakan menjadi 2, yakni reaksi satu arah (irreversible) dan reaksi dua arah (reversible). Berikut ini penjelasan dari reaksi-reaksi yang dimaksud tersebut: a.

Kesetimbangan Dinamis YouTube
Reaksi kesetimbangan terjadi ketika reaksinya bolak-balik (reversibel), sistemnya tertutup, dan bersifat dinamis. Bersifat dinamis berarti secara mikroskopis reaksi berlangsung terus-menerus dalam dua arah dengan laju reaksi pembentukan sama dengan laju reaksi baliknya. Berlangsungnya suatu reaksi secara makroskopis dapat dilihat dari perubahan.

Kimia Dasar (4) sistem kesetimbangan heterogen
Nah, hal ini disebut dengan kesetimbangan dinamis karena ada perubahan dua arah. Air yang direbus dalam panci tertutup (Sumber: wikipedia.org) Kesetimbangan dinamis bekerja saat kecepatan reaksi pembentukan produk sama dengan kecepatan pembentukan reaktan. Ingat, dalam kesetimbangan dinamis akan selalu ada perubahan menuju produk dan perubahan.