
Contoh Reaksi Reduksi Dan Oksidasi Berdasarkan Perubahan Bilangan Oksidasi Sketsa
Pada mulanya reaksi oksidasi diartikan sebagai reaksi pengikatan oksigen oleh zat tertentu. Sedangkan reaksi reduksi adalah reaksi pelepasan oksigen. Contoh reaksinya yaitu: Oksidasi : H 2 (g) + ½ O 2 (g) → H 2 (l) Reduksi : FeO (s) + CO (g) → Fe (s) CO 2 (g) Namun pendapat tersebut dinilai kurang menjelaskan reaksi kimia secara luas.

Peristiwa Reduksi Terdapat Pada Perubahan Sinau
Oksidasi dan reduksi tepatnya merujuk kepada perubahan bilangan oksidasi karena transfer elektron yang sebenarnya tidak akan selalu terjadi.. Dalam praktiknya, transfer elektron akan selalu mengubah bilangan oksidasi, tetapi terdapat banyak reaksi yang diklasifikasikan sebagai "redoks", walaupun tidak ada transfer elektron dalam reaksi.
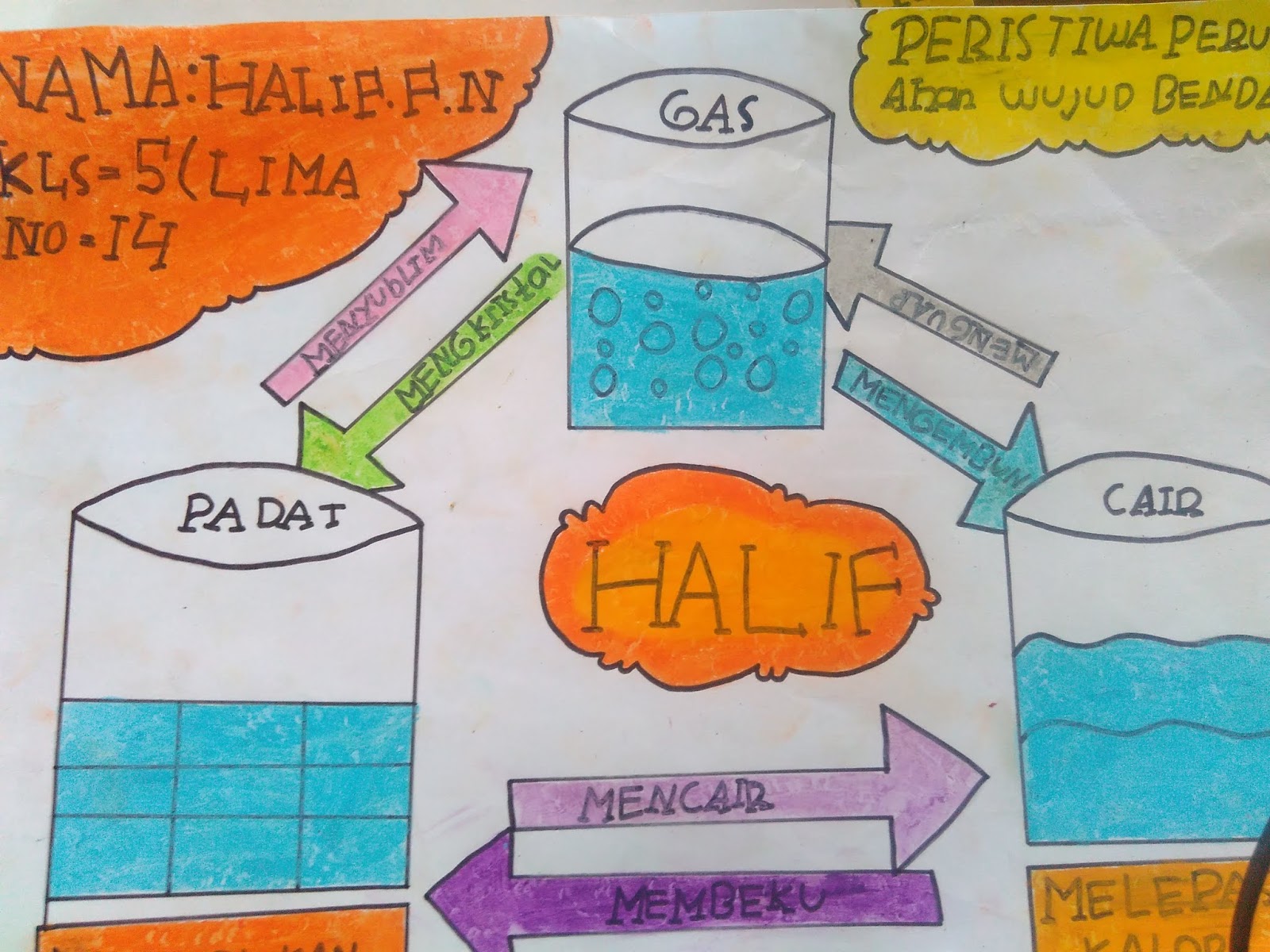
Poster Peristiwa Perubahan Wujud Benda
Pada masing-masing perubahan berikut, tentukan peristiwa oksidasi atau reduksi dan berikan alasannya. A . CrO 2 − menjadi CrO 4 2 − B . BaSO 4 menjadi BaS C . H 2 S menjadi S D . OCl − menjadi CIO 3 − E . AsH 3 menjadi H 3 AsO 4

Peristiwa Reduksi Terdapat Pada Perubahan Ilustrasi
Reaksi redoks merupakan reaksi yang terdiri dari reduksi dan oksidasi. Banyak sekali contoh reaksi redoks yang terjadi dalam kehidupan di sekitarmu. Seperti peristiwa perkaratan pada paku besi, perubahan warna pada buah apel dan pisang setelah dikupas, dan masih banyak lagi. Dalam reaksi redoks terdapat istilah reduktor dan oksidator.

Peristiwa Reduksi Terdapat Pada Perubahan Sinau
KOMPAS.com - Reduksi adalah kegiatan untuk mengurangi sesuatu. Dalam ilmu kimia juga terjadi reaksi reduksi yang berhubungan dengan kandungan oksigen suatu zat.. Dilansir dari Encyclopedia Britannica, reaksi reduksi adalah penurunan bilangan oksidasi suatu zat karena kehilangan atau melepaskan oksigen.. Saat reaksi reduksi terjadi, zat akan mengalami kenaikan elektron sehingga membuatnya lebih.

Oksidasi dan Reduksi Ilmu Kimia
Hal itu dikarenakan tidak terdapat perubahan total muatan selama reaksi redoks, total elektron yang berlebihan ada reaksi oksidasi wajib sama dengan jumlah yang dikonsumsi ada reaksi reduksi.. Pada reduksi terdapat peristiwa diperolehnya elektron, atau menurunnya bilangan oksidasi suatu atom, molekul, atau ion. Sementara reduktor merupakan.

Peristiwa Reduksi Terdapat Pada Perubahan Ilustrasi
Dalam buku Ilmu Pengetahuan Alam dan Sosial untuk SD Kelas IV, transformasi energi adalah perubahan bentuk energi yang digunakan manusia untuk memanfaatkan energi. Pada pelajaran IPAS kelas 4 SD Kurikulum Merdeka Belajar, kita akan belajar menyebutkan contoh peristiwa perubahan energi gerak menjadi energi bunyi.

Peristiwa Reduksi Terdapat Pada Perubahan Sinau
Berdasarkan penangkapan atau pelepasan oksigen. Oksidasi: reaksi yang melibatkan penangkapan atom oksigen. Contoh: C+ O2 → CO2. Atom C (karbon) mengalami oksidasi karena dalam reaksi atom karbon mengikat atom oksigen menjadi CO2. Reduksi: reaksi yang melibatkan pelepasan atom oksigen. Contoh: H2O2 → H2O + O2.
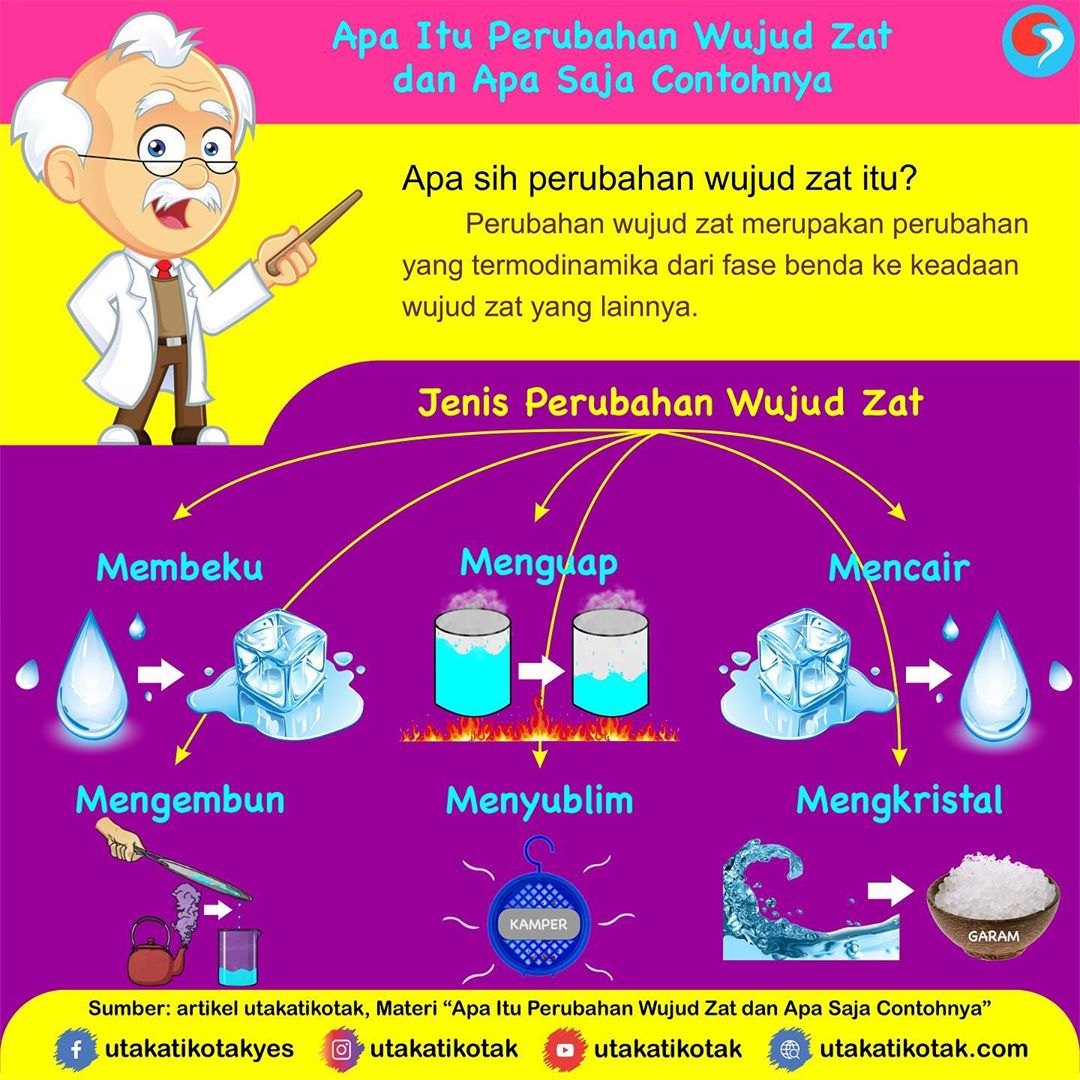
Perubahan Wujud Benda dan Contohnya
Ciri-ciri Reaksi Redoks. Adapun ciri-ciri reaksi redoks yang dijelaskan dalam sumber di atas, yaitu: 1. Ada unsur bebas misalnya Cl2 (Klorin), Cu (Cuprum), dan O2 (Oksigen). 2. Terjadi perubahan biloks (bilangan oksidasi). 3. Ada reduktor (pereduksi) adalah suatu zat yang mengalami oksidasi. 4.

Peristiwa Reduksi Terdapat Pada Perubahan ikon gambar icon dan fungsinya
Contoh reduksi ada dalam pengolahan bijih besi (Fe2O3) menjadi besi dengan suhu tinggi, yang menggunakan CO (karbonmonoksida). Dalam proses reduksi di pengolahan bijih besi menjadi besi reaksinya adalah: Fe2O3(s) + 3 CO(g) → 2Fe(s) + 3 CO2(g). 2. Konsep Reaksi Redoks Berdasarkan Transfer Elektron
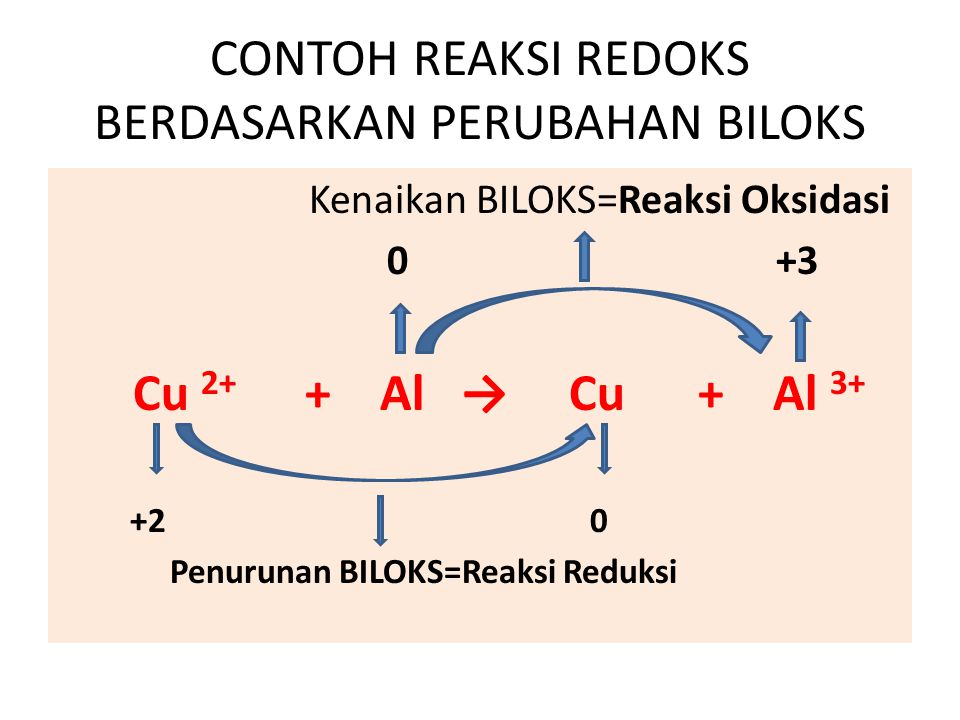
Contoh Reaksi Reduksi Dan Oksidasi Berdasarkan Perubahan Bilangan Oksidasi Sketsa
20 questions. 1. Multiple Choice. Pada reaksi redoks, spesies yang mengalami peristiwa oksidasi adalah…. 2. Multiple Choice. Pernyataan yang tidak benar tentang reaksi reduksi berikut adalah…. 3. Multiple Choice.

Peristiwa Reduksi Terdapat Pada Perubahan Sinau
Oke, kita lanjut ya bahasannya! Pada reaksi redoks, terdapat unsur-unsur yang bertindak sebagai reduktor dan oksidator. Zat yang mengalami oksidasi itu disebut reduktor, sedangkan zat yang mengalami reduksi disebut oksidator. Coba perhatikan contoh berikut ini, ya! Reaksi: Mg(s) + 2HCl -----> MgCl2(aq) + H2(g) Karena Mg merupakan unsur bebas, jadi biloks Mg = 0.

Mempelajari Konsep Reaksi Redoks (ReduksiOksidasi) Kimia Kelas 10
Jakarta - . Reaksi redoks adalah reaksi kimia yang terjadi dari gabungan reduksi dan reaksi oksidasi. Reaksi redoks mencakup semua proses kimia, di mana atom melibatkan perubahan keadaan bilangan oksidasi (biloks). Pada suatu reaksi kimia yang lengkap, reaksi oksidasi akan selalu diikuti oleh reaksi reduksi, sehingga reaksi yang terjadi dikenal dengan istilah reaksi redoks.

Peristiwa Reduksi Terdapat Pada Perubahan Sinau
Penjelasan Lengkap Reaksi Redoks (Reduksi dan Oksidasi) LENGKAP. Daftar Isi+. Reaksi redoks adalah reaksikimia yang menyebabkan adanya perubahan bilangan oksidasi pada suatu unsur, maupun molekul. Dalam kehidupan sehari-hari seringkali terjadi reaksi redoks. Diantaranya adalah besi yang berkarat, sayuran yang membusuk.

Peristiwa Reduksi Terdapat Pada Perubahan Sinau
Pengertian Reaksi Redoks. Redoks adalah istilah yang menjelaskan perubahan bilangan oksidasi dalam sebuah reaksi kimia. Nah, lebih lanjut, hal ini dapat berupa reaksi redoks sederhana seperti oksidasi karbon yang menghasilkan karbon dioksida (CO2), atau reduksi karbon oleh hidrogen sehingga menghasilkan metana (CH4), ataupun dapat berupa proses kompleks seperti oksidasi gula pada tubuh manusia.

Peristiwa Reduksi Terdapat Pada Perubahan Ilustrasi
Reaksi redoks, singkatan dari "reaksi reduksi-oksidasi," adalah salah satu jenis reaksi kimia yang sangat penting dalam dunia ilmu kimia. Dalam reaksi ini, terjadi pertukaran elektron antara atom atau molekul yang terlibut, menyebabkan perubahan pada bilangan oksidasi, yang kemudian memengaruhi sifat-sifat zat-zat yang terlibat.