
Penjelasan Endoterm dan Eksoterm dalam termokimia YouTube
Penyebab terjadinya peristiwa mencair adalah karena suatu benda mengalami pemanasan atau peningkatan suhu. Contohnya yakni pada es batu dan es krim yang dibiarkan di cuaca panas, serta lilin yang dinyalakan. 3. Menguap. Menguap adalah peristiwa perubahan wujud dari cair menjadi gas. Peristiwa ini terjadi karena peningkatan atau pemanasan suhu.

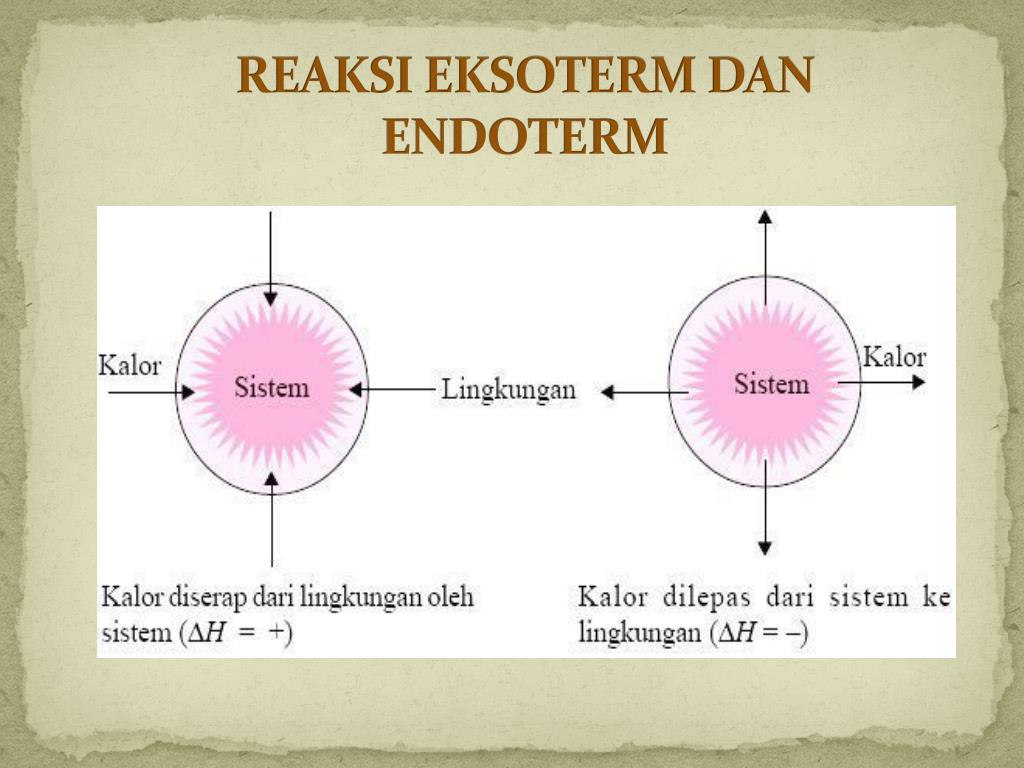
Reaksi Eksoterm Dan Endoterm
Reaksi eksoterm merupakan suatu reaksi kimia yang menghasilkan kalor, sedangkan reaksi endoterm merupakan reaksi penyerapan kalor.. Salah satu peristiwa eksotermik adalah adanya pembakaran (Experience Life) Cari soal sekolah lainnya. KOMPAS.com - Reaksi eksoterm dan endoterm adalah dua jenis perubahan kimia dibedakan berdasarkan nilai.
PPT TERMOKIMIA PowerPoint Presentation, free download ID3164513
Untuk keterangan lebih lanjut, klik [tampil] di bagian kanan. Reaksi eksoterm adalah kalor yang dihasilkan oleh suatu proses pembakaran dipindahkan dari sistem ke lingkungannya. [1] Dengan kata lain yaitu suatu reaksi yang menghasilkan kalor . Sebagai contoh yaitu pada reaksi pembakaran yang terjadi pada api adalah reaksi eksoterm sehingga akan.

VIRTUAL EXPERIMENT REAKSI EKSOTERM NaOH dan HCl YouTube
Praktikum Reaksi Eksoterm dan Reaksi Endoterm Judul Kegiatan : Reaksi Eksoterm dan Reaksi Endoterm Tujuan :untuk mengetahui reaksi eksoterm dan reaksi endoterm.. Peristiwa yang terjadi pada sel-sel umbi kentang berakibat dua hal : 1. Sel-sel kentang kekurangan air (isi sel), akibatnya terjadi plasmolisis yang mengakibatkan penurununan.

Contoh Peristiwa Eksoterm Dalam Kehidupan Sehari hari YouTube
cara mudah menentukan reaksi yang termasuk eksoterm dan endoterm jika diketahui peristiwa dalam kehidupan sehari-hari es batu mencair, kembang api terbakar,.

Amazing Experience with Chemistry Reaksi Eksoterm dan Endoterm
Reaksi eksoterm: entalpi energi produk lebih kecil daripada entalpi energi reaktan ( Δ H = H produk − H reaktan, Δ H = −). Salah. I 2 ( g) + 3 Cl 2 ( g) → 2 ICl 3 ( s) Δ H = − 214 kJ/mol. Reaksi eksoterm terjadi pelepasan energi dari sistem ke lingkungan sehingga suhu campuran (setelah reaksi) bertambah.

Eksoterm Endoterm Sinau
Salah satu contoh reaksi endoterm dalam kehidupan sehari-hari adalah peristiwa fotosintesis. Dalam peristiwa ini, pepohonan menyerap kalor yang berasal dari matahari yang kemudian menaikan entalpi reaksinya. Sistem dan Lingkungan. Dalam pembahasan pengertian eksoterm dan endoterm di atas kamu menemukan istilah "sistem" dan "lingkungan".

Termokimia Sistem Lingkungan Reaksi Eksoterm Endoterm Perubahan Entalpi Standar YouTube
Reaksi endoterm dan eksoterm adalah reaksi kimia yang masing-masing menyerap dan melepaskan panas. Contoh reaksi endoterm yang baik adalah fotosintesis. Pembakaran adalah contoh reaksi eksoterm. Kategorisasi reaksi sebagai endo- atau eksotermik tergantung pada perpindahan panas bersih. Dalam setiap reaksi tertentu, panas diserap dan dilepaskan.

REAKSI ENDOTERM & EKSOTERM TERMOKIMIA YouTube
Eksotermik ("pemanasan luar") dalam kaidah pembahasan termodinamika menjelaskan suatu proses atau reaksi yang melepaskan energi panas atau energi cahaya (contohnya percikan api atau ledakan), energi listrik (contohnya pada baterai ), atau bisa juga energi suara. Asal kata eksotermik adalah dari awalan kata bahasa Yunani " ex -" (yang berarti di.

Termokimia Perbedaan Reaksi Eksoterm dengan Reaksi Endoterm YouTube
Perbedaan Reaksi Endoterm dan Eksoterm. Salah satu peristiwa eksotermik adalah adanya pembakaran (Experience Life) KOMPAS.com - Dalam termokimia, reaksi kimia dapat melepaskan atau menyerap energi berupa panas dari lingkungannya. Reaksi kimia tersebut dibagi menjadi dua, ialah reaksi endoterm dan reaksi eksoterm.

Eksoterm dan Endoterm ( TERMOKIMIA) KIMIA SMA YouTube
Pada reaksi eksoterm, tanda panah mengarah ke bawah. Arah tanda panah selalu menunjuk ke arah produk. H produk < H reaktan sehingga dirumuskan ∆H = Hp - HR < 0 atau ∆H bernilai negatif. C. Peristiwa Eksoterm Dalam Kehidupan Sehari-hari. Reaksi pembakaran (kayu, bensin, dan lain-lain) Reaksi perkaratan besi; Reaksi respirasi (pernapasan)

Gambar Reaksi Eksoterm Dan Endoterm Ilmu
Reaksi endoterm menyerap sejumlah energi sehingga energi sistem bertambah. Karena entalpi bertambah, perubahan entalpinya bertanda positif. [3] Dapat dijelaskan dengan gambar sebagai berikut. Pada reaksi endoterm, sistem menyerap energi. Oleh karena itu, entalpi sistem akan bertambah. Artinya, entalpi produk (Hp) lebih besar daripada entalpi.

Contoh Reaksi Eksoterm YouTube
Pada contoh di atas yang termasuk lingkungan adalah bagian selain reaktan dan produk, misalnya udara di sekitarnya. Nah, reaksi eksoterm merupakan reaksi pembebasan kalor dari sistem ke lingkungan sehingga suhu lingkungan bertambah (mengalami kenaikan, T2 > T1). Pada reaksi eksoterm, sistem yang melepaskan kalor akan mengalami penurunan energi.

Termokimia (Entalpi, Reaksi eksoterm dan endoterm) YouTube
Ciri-ciri reaksi eksotermik adalah adanya kalor dari sistem yang diserap oleh lingkungan. Dalam reaksi eksotermik, kalor atau penas dilepaskan saat reaksi terjadi. Hal ini membuat jumlah kalor lingkungan lebih rendah daripada jumlah kalor sistem. Sehingga, lingkungan akan menyerap kalor yang dilepaskan sistem dan sistem akan terasa panas.

SAINS Reaksi Eksoterm dan Reaksi Endoterm
Reaksi eksoterm adalah reaksi yang menyebabkan adanya transfer kalor dari sistem ke lingkungan. Reaksi eksoterm selalu ditandai dengan adanya kenaikan suhu sistem saat reaksi berlangsung. Perubahan entalpi dihitung dengan. ΔH = energi untuk memutus ikatan - energi untuk membuat produk reaksi. Dengan demikian, perubahan entalpi bertanda.

Perbedaan Reaksi Eksoterm dan Endoterm Ilmu Kimia
Jakarta - . Reaksi eksoterm adalah reaksi yang terjadi dengan melepaskan kalor ke lingkungan. Pada reaksi ini, terjadi perpindahan kalor dari sistem ke lingkungan sehingga menjadi panas. Reaksi eksoterm akan membebaskan energi, sehingga entalpi sistem berkurang dan perubahan entalpi bernilai negatif, seperti dikutip dari buku Cerdas Belajar Kimia oleh Nana Sutresna.