
Trik Menentukan Pasangan Asam Basa Konjugasi KIMIA OKE PINTAR
Baca juga: Daftar Nama Asam-Basa Kuat dan Asam-Basa Lemah. Reaksi bersifat ireversibel atau bolak-balik. Di mana ion Cl- dapat kembali menerima proton dari H3O+ (air yang menerima proton) dan berubah kembali menjadi HCl. Adapun, contoh pasangan asam dan basa konjugasi Bronsted Lowry adalah: Senyawa Asam.

Contoh Soal menentukan pasangan asam basa konjugasi menurut BronstedLowry YouTube
Teori asam basa Bronsted Lowry menjelaskan rumus kimia dari pasangan asam basa konjugasi dan hanya berbeda satu proton H+ saja. Reaksi di bawah HCl merupakan asam karena telah memberikan proton serta NH3 serta merupakan basa karena menerima proton. Sementara ion Cl- adalah basa konjugasi dari HCl dan NH4+ adalah asam konjugat dari NH3.

Asam dan Basa Konjugasi
Dengan kata lain, asam konjugasi adalah anggota asam, HX, dari sepasang senyawa yang berbeda satu sama lain dengan mendapatkan atau kehilangan proton. Asam konjugasi dapat melepaskan atau menyumbangkan proton. Basa konjugasi adalah nama yang diberikan untuk spesies yang tersisa setelah asam menyumbangkan protonnya.
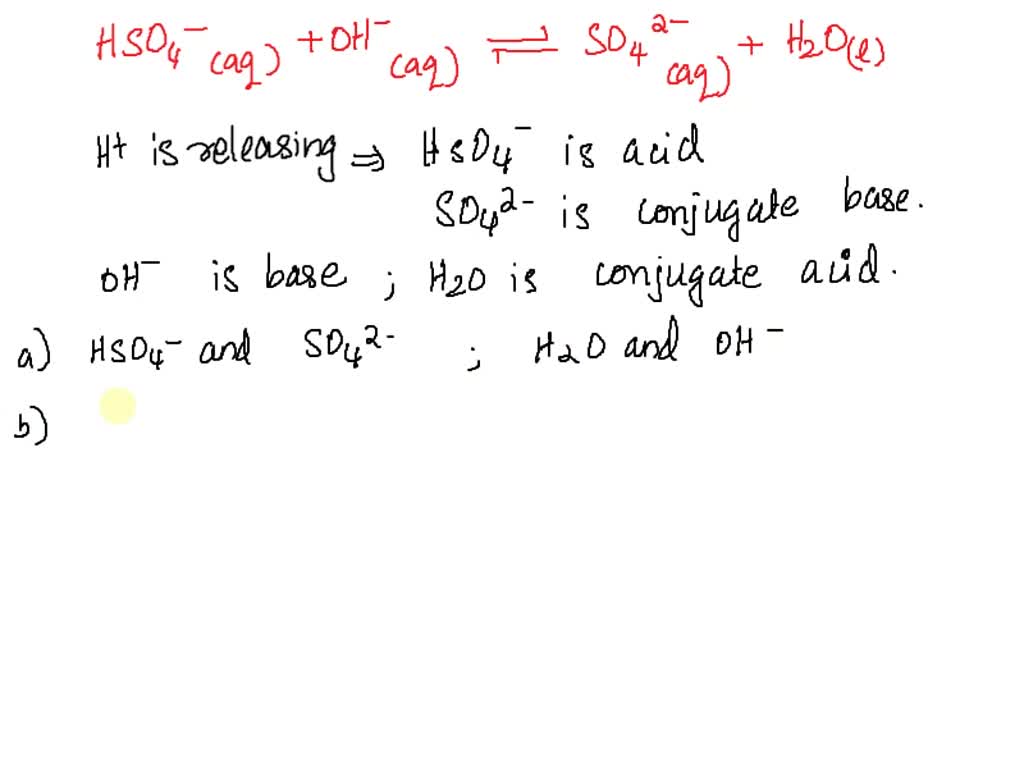
SOLVED pasangan asam basa konjugasi dari reaksi hso4(aq) + h2o(l) = h3o+(aq) + so4 2(aq) adalah
Asam konjugasi adalah basa yang memperoleh ion hidrogen, sedangkan basa konjugasi adalah yang tersisa setelah asam memberikan proton dalam sebuah reaksi kimia. Kedua hal tersebut disebut pasangan asam basa konjugasi. Teori Asam Basa Lewis. Asam basa Lewis menjelaskan terkait struktur dan ikatannya.

Cara Mencari Pasangan Asam Basa Menurut Teori Bronsted Lowry AsamBasa YouTube
#"Acid + Base "rightleftharpoons" Conjugate base + conjugate acid"# And so we got.. #underbrace(NH_3(aq))_"base" + H_2O(l) rightleftharpoonsunderbrace(NH_4.

Contoh Asam Basa Menurut Bronsted Lowry Berbagai Contoh Riset
Dari gambar terlihat bahwa air yang telah melepaskan proton berubahn menjadi basa konjugasi OH-. Dan ammonia (NH3) yang telah menerima donor proton berubah menjadi asam konjugasi NH4+. Sehingga pasangan asam basa konjugasinya adalah H2O dan NH3, juga OH- dan NH4+. Kita dapat menentukan mana asam konjugasi mana basa konjugasi dari reaksi.

LENGKAP ‼️ Cara Mudah Menentukan Pasangan Asam Basa Konjugasi TeoriAsamBasa AsamBasaKonjugasi
Basa konjugasi merupakan produk yang dihasilkan setelah suatu asam melepaskan ion H+. Untuk reaksi di atas, maka CH3COOH (asam1) dengan CHCOO (basa2) merupakan pasangan asam-basa konjugasi. Begitu juga pasangan asam2 dan basa2. Secara sederhana, teori ini dapat dituliskan sebagai berikut: Asam ⇌ H+ + basa konjugasi.

Tentukan Pasangan Asam Basa Konjugasi Dari Reaksi Berikut Homecare24
Pasangan asam basa konjugasi: 1. adalah asam konjugasi karena memberikan ion (proton donor) kepada molekul dan berubah menjadi .. Berdasarkan penjelasan tersebut maka pasangan asam basa konjugasi pada reaksi adalah. Jadi, jawaban yang benar adalah E. Perdalam pemahamanmu bersama Master Teacher di sesi Live Teaching, GRATIS! 99.

Menentukan Pasangan Asam Basa Konjugasi Teori Asam Basa BronstedLowry / kimia kelas 11 YouTube
HNO 3 adalah asam.HNO 3 melepas proton (H+) menjadi NO 3 - yang merupakan basa konjugasi. H 2 O adalah basa.H 2 O menerima proton (H+) menjadi H 3 O + yang merupakan asam konjugasi.. Maka, HNO 3 dan NO 3 - merupakan pasangan asam basa konjugasi. Serta, H 2 O dan H 3 O + merupakan pasangan asam basa konjugasi. [inline_ads] 3. Zat Amfoter. Zat amfoter adalah suatu zat yang berperan sebagai.

Pasangan Asam Basa Konjugasi H2O + HNO2 YouTube
Menurut Bronsted Lowry asam adalah spesies apa pun yang menyumbangkan proton (H+). Dilansir dari Chemistry LibreTexts, asam yang kehilangan proton berubah menjadi basa konjugasinya. Misalnya, senyawa asam Bronsted HF yang direaksikan dengan air dengan reaksi berikut: HF (aq) + H2O (l) → F- (aq) + H2O+ (aq). Dalam reaksi tersebut, proton dari.

Pasangan asam basa konjugasi dari reaksi HSO+H20 H3O+S...
Asam konjugasi menurut teori asam-basa Brønsted-Lowry dibentuk oleh penerimaan proton (H +) oleh basa; dalam kata lain, asam konjugasi adalah basa yang telah memperoleh ion hidrogen.Di sisi lain, basa konjugasi adalah yang tersisa setelah asam telah memberikan proton dalam suatu reaksi kimia. Maka dari itu, basa konjugasi dibentuk oleh pelepasan proton dari suatu asam.

Tunjukkan pasangan asam basa konjugasi pada reaksi...
Asam lemah: HA + H 2 O ⇌ H 3 O + + A - (basa kuat) Basa sesaat setelah menerima proton akan berubah menjadi asam konjugasi dari basa tersebut. Contoh tipe reaksi: Basa kuat: B + H + → BH + (asam lemah) Bila ditulis secara lengkap: Basa kuat: B + H 3 O + → BH + (asam lemah) + H 2 O. Basa lemah: B + H + ⇌ BH + (asam kuat) Bila ditulis.

PPT TEORI ASAM BASA PowerPoint Presentation, free download ID5368090
Alkafirun pada saat kali ini telah disediakan sebuah reaksi bolak-balik dan kita diminta untuk menentukan pasangan asam basa konjugasinya sebelumnya pasangan asam basa konjugasi adalah pasangan asam basa yang berbeda 1 H plus Jadi jika ada sebuah asam X maka basa konjugat nya adalah x min 1 H plus dan jika ada basa maka asam konjugat nya adalah y ditambah 1 + untuk reaksi pada soal ini CH3COOH.

Tentukan pasangan asam basa konjugasi pada reaksi berikut...
Pasangan asam basa konjugasi adalah konsep penting dalam kimia yang membantu kita memahami bagaimana zat-zat tersebut berinteraksi satu sama lain. Definisi, sifat, dan contoh-contoh pasangan asam basa konjugasi menjelaskan hubungan antara asam dan basa dalam reaksi kimia. Memahami konsep ini dengan baik akan membantu dalam mempelajari reaksi.
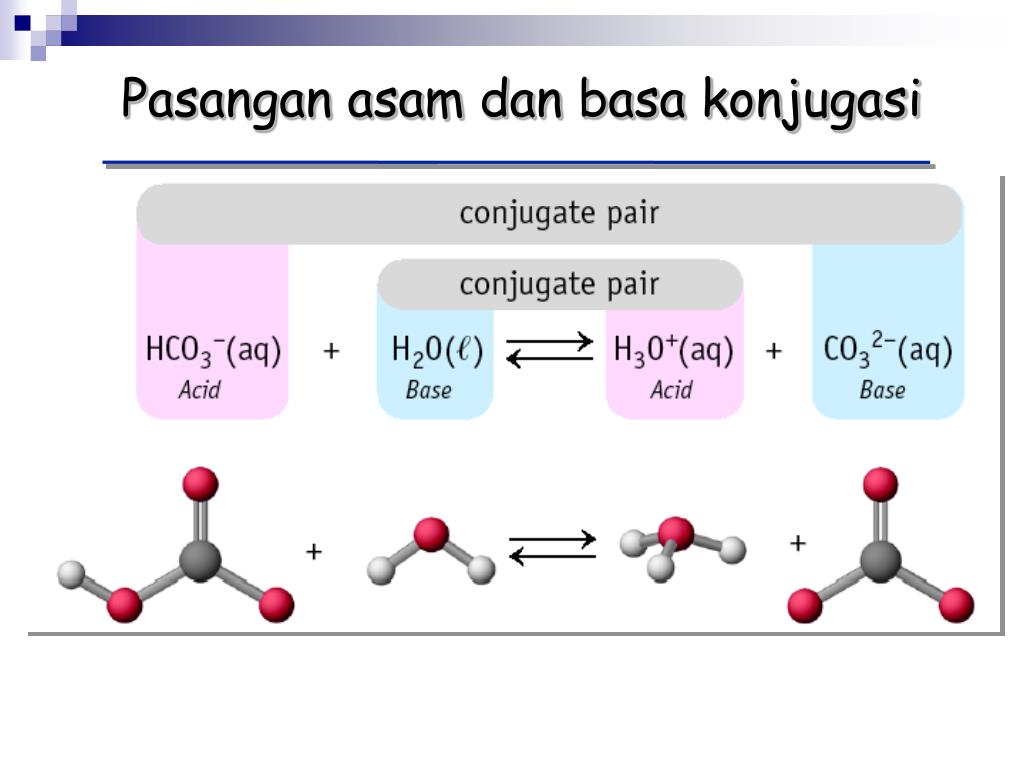
PPT ASAM DAN BASA PowerPoint Presentation, free download ID1244635
H 2 O dan H 3 O + merupakan pasangan asam-basa konjugasi. H 2 O adalah basa konjugasi dari H 3 O + dan H 3 O + adalah asam konjugasi dari H 2 O. Contoh Soal Asam dan Basa Konjugasi. Berikut ini contoh pasangan asam-basa konjugasi pada beberapa reaksi. a. HNO 3(aq) + H 2 O (l) ⇄H 3 O + (aq) + NO 3.

Cara mencari Pasangan AsamBasa konjugasi AsamBasa YouTube
Jika basa konjugat lebih stabil dari asam, maka asam akan cenderung berdisosiasi dan menjadi lebih kuat, sedangkan jika sebaliknya maka akan menjadi asam lemah. Contoh asam:pasangan basa konjugasi. Berikut adalah beberapa contoh tambahan dari berbagai asam dan basa konjugatnya masing-masing: Asam klorida dan anion klorida (HCl dan Cl -)