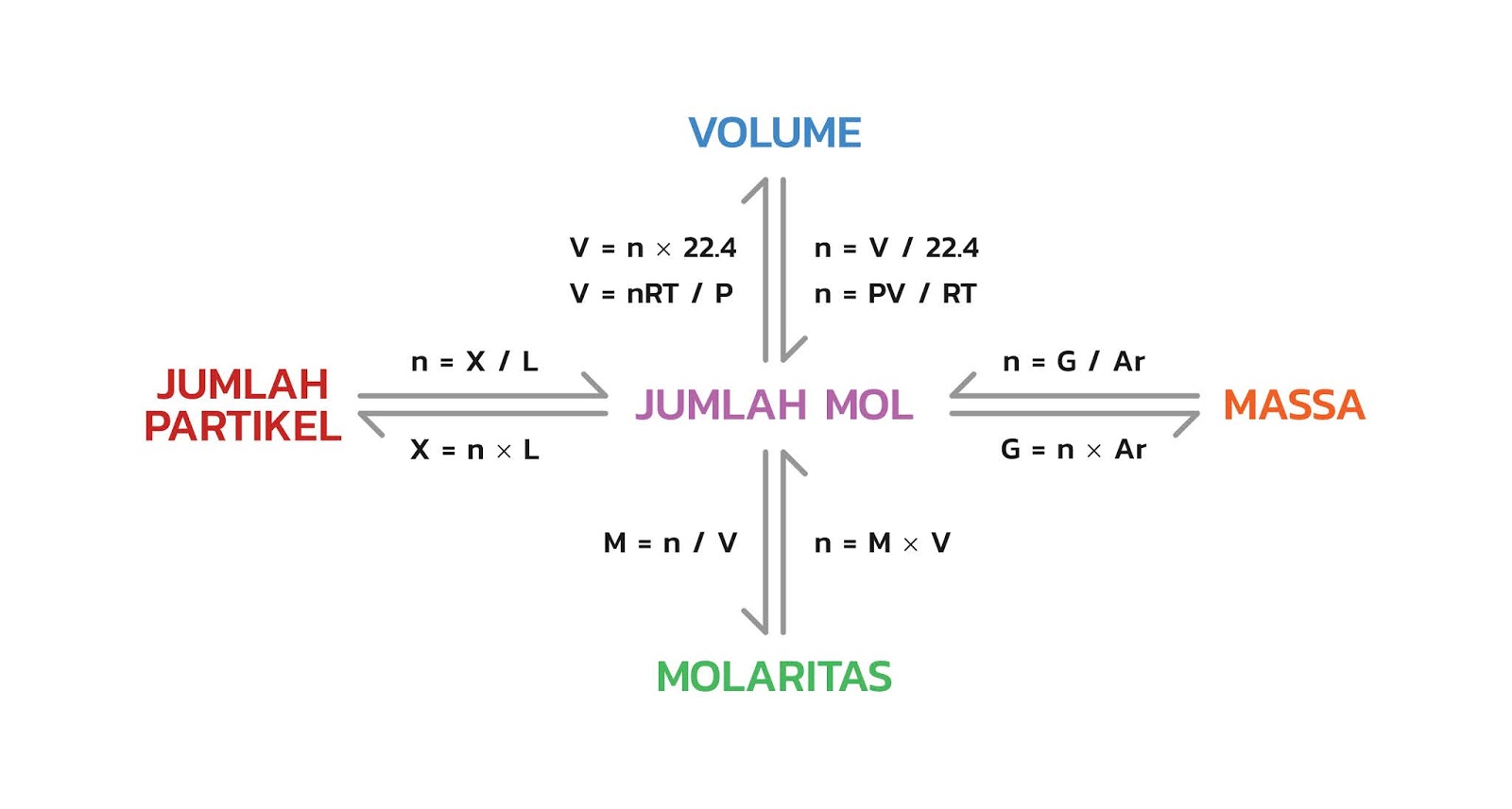
Hubungan Mol Dengan Jumlah Partikel Massa Volume Dan Molaritas Riset
1 mol adalah satuan jumlah zat dalam kimia, yang setara dengan 6,022 x 10²³ partikel.. 1 mol adalah sebuah satuan ukuran dalam kimia yang digunakan untuk mengukur banyaknya zat dari molekul, atom, atau ion tertentu di mana 1 mol yang dikandung oleh suatu zat sama dengan jumlah partikel dasar atau molekul sebanyak 6,022 x 10^23 buah.

Soal Konsep Mol Bilangan Avogadro = 6,02 x 10^23 maka 0,5 mol air mengandung Berapa Molekul
Konsep mol didukung oleh adanya bilangan Avogadro yang ditemukan oleh fisikawan italia bernama Amadeo Avogadro. Bilangan Avogadro menyatakan bahwa dalam satu mol zat, terdapat partikel sejumlah 6,02214076x10^23. Baca juga: Pengertian dan Contoh Soal Fraksi Mol. Contohnya adalah 1 mol air mengandung 6,02214076x10^23 partikel air, sangat banyak.

Rumus Fraksi Mol Pengertian, Sifat dan Contoh Soalnya Lengkap BprsKu.Co.Id
Antara solut dan solven memiliki partikel-partikel sebesar molekul atau ion. Nah, antar partikelnya tersebar secara merata dan homogen. Di dalam Kimia, banyaknya zat seringkali dinyatakan dalam besaran mol. Mol ini yang nantinya akan digunakan untuk menghitung konsentrasi molaritas dan molalitas.. molalitas adalah besaran yang menyatakan.

Pengertian Mol Konsep dan Penggunaannya dalam Kimia
Mol (simbol: mol; bahasa Inggris dan Prancis: mole) adalah satuan pokok untuk besaran jumlah zat dalam Sistem Satuan Internasional (SI). Setelah redefinisi pada tahun 2019, definisi satuan mol, seperti yang disebutkan dalam Brosur SI edisi kesembilan, adalah sebagai berikut.. Mol, yang disimbolkan dengan mol, adalah satuan jumlah zat dalam SI. Satu mol mengandung persis 6,022140 76 × 10 23.

STOIKIOMETRI Pengertian Konsep mol Stoikiometri Konsep Mol satuan
Jadi, persentase massa unsur C di dalam glukosa adalah 40%. Mudah, bukan? Pengertian Mol. Mol merupakan jumlah tertentu untuk menyatakan banyaknya suatu zat yang berukuran mikroskopis. Satu mol menunjukkan banyaknya partikel yang terkandung dalam suatu zat yang jumlahnya sama dengan jumlah partikel dalam 12 gram atom C-12.
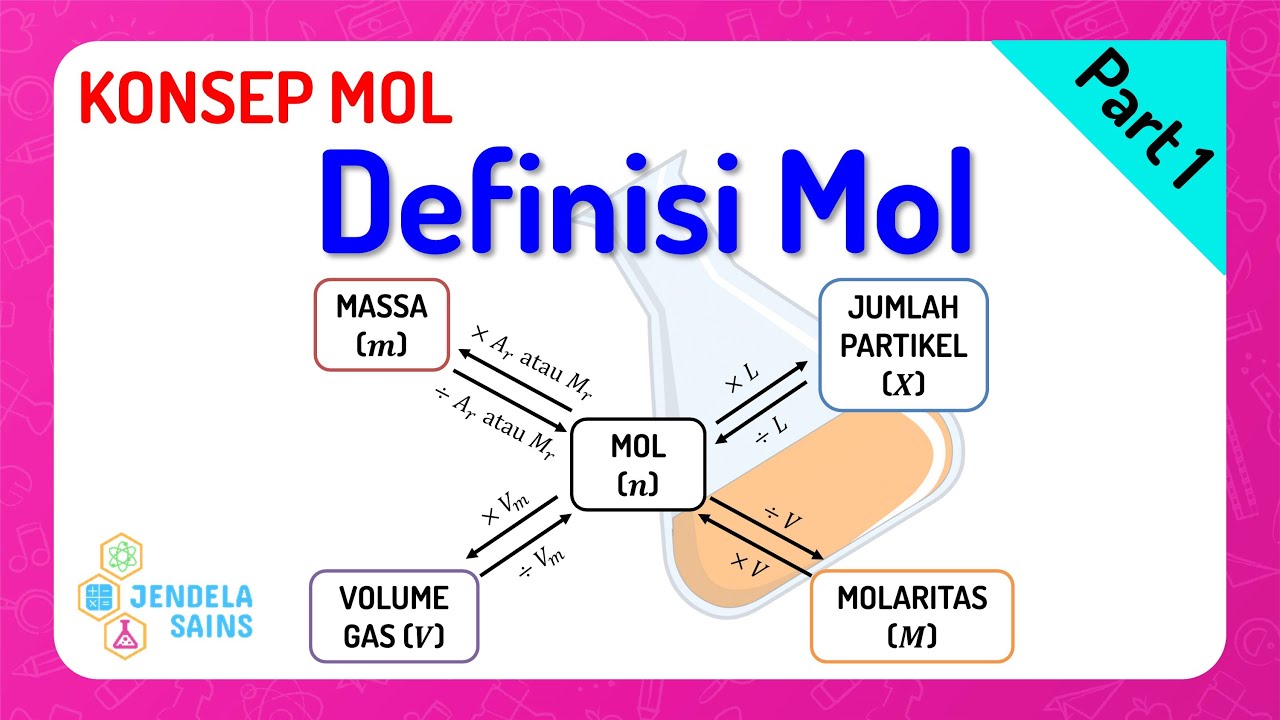
Konsep Mol Kimia Kelas 10 • Part 1 Hubungan Mol & Massa, Jumlah Partikel, Volume Gas, Molaritas
Mol adalah satuan umum yang dapat menyatakan jumlah partikel dalam zat. Massa setiap zat dalam 1 mol tidak sama maka perlu ada penghubung antara massa zat dengan jumlah partikel.. Satu mol menunjukkan banyaknya partikel yang terkandung dalam suatu zat yang jumlahnya sama dengan jumlah partikel dalam 12 gram atom C-12. Satu mol materi.

Konsep Mol Part1 (Mol, Jumlah Partikel dan Massa) YouTube
Banyaknya partikel dinyatakan dalam satuan mol. Satuan mol sekarang dinyatakan sebagai jumlah patikel (atom, molekul, atau ion) dalam suatu zat. Para ahli sepakat bahwa satu mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12,0 gram isotop C-12 yakni 6,02 x 1023 partikel.

HUBUNGAN ANTARA MASSA, JUMLAH MOL, DAN JUMLAH PARTIKEL
Hubungan Mol dengan Jumlah Partikel. Seperti yang udah kalian tahu nih, 1 mol menyatakan banyaknya partikel dalam suatu zat, yang mana jumlahnya sama dengan jumlah partikel dalam 12 g atom C-12. Berdasarkan penelitian pak Avogadro diketahui nih kalau dalam 1 mol atau 12 g atom C-12 terkandung 6,02 x 10²³ partikel.

1. Hubungan mol dg jumlah partikel YouTube
Satu mol adalah jumlah partikel yang terkandung dalam suatu zat yang jumlahnya sama dengan partikel yang terdapat dalam 12 gram atom C-12. Banyaknya atom yang terdapat dalam 12 gr C-12 adalah 6,02 x 10 23 partikel yang disebut dengan tetapan Avogadro dan dinyatak dengan huruf L. Dalam ketentuan tersebut, partikel dapat berupa atom, molekul, maupun ion.

Soal Kimia Tentang Konsep Mol Satuan Jumlah Zat Read Master
Mol (simbol: mol; bahasa Inggris dan Prancis: mole) adalah satuan pokok untuk besaran jumlah zat dalam Sistem Satuan Internasional (SI). Setelah redefinisi pada tahun 2019, definisi satuan mol, seperti yang disebutkan dalam Brosur SI edisi kesembilan, adalah sebagai berikut. [1] Mol, yang disimbolkan dengan mol, adalah satuan jumlah zat dalam SI. Satu mol mengandung persis 6,022140 76 × 10 23.
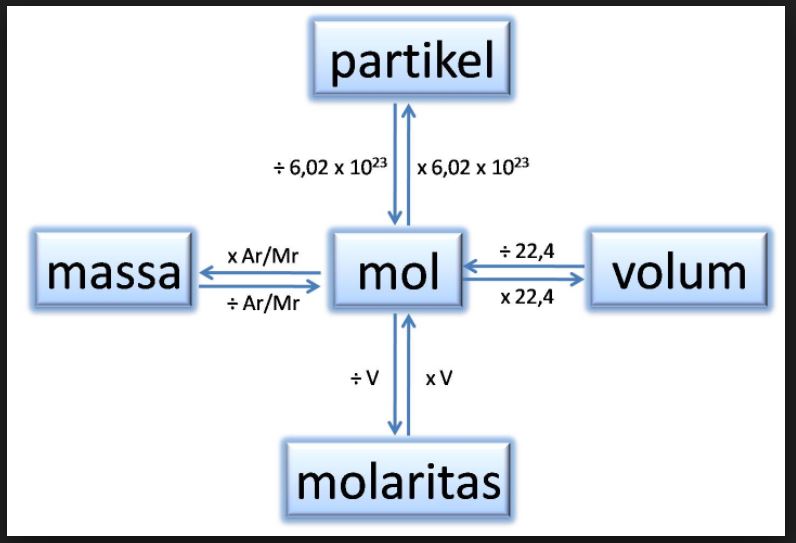
Hubungan Mol dengan Jumlah Partikel dan Massa Zat Read HSTKB
Analisa Konsep Mol Hubungan Mol dengan Jumlah Partikel Satu mol zat apapun akan memiliki jumlah partikel yang sama, yaitu sebesar 6,02 1023 partikel. Misalnya: 1 mol air mengandung 6,02 1023 molekul H2O 1 mol gas oksigen mengandung 6,02 1023 molekul O2 1 mol natrium mengandung 6,02 1023 atom Na

Konsep Mol dan Analisanya
Memahami konsep mol penting dalam kimia karena dapat membantu kita memahami bagaimana partikel-partikel tersebut bereaksi dalam reaksi kimia dan bagaimana menghitung jumlah partikel yang terlibat dalam suatu reaksi.. Selain itu, penggunaan satuan mol juga sangat umum dalam kehidupan sehari-hari, seperti dalam bidang farmasi, industri, dan lain sebagainya.

Rumus Gas Ideal Riset
Konsep mol adalah Ide atau pengertian mengenai mol, yakni satuan jumlah suatu zat. Jumlah mol dinyatakan dengan simbol n Banyaknya atom atau partikel yang terdapat dalam 12 gram C-12 adalah $6,02\times10^{23}$ partikel yang disebut dengan tetapan Avogadro yang dinyatakan dengan simbol L atau NA.
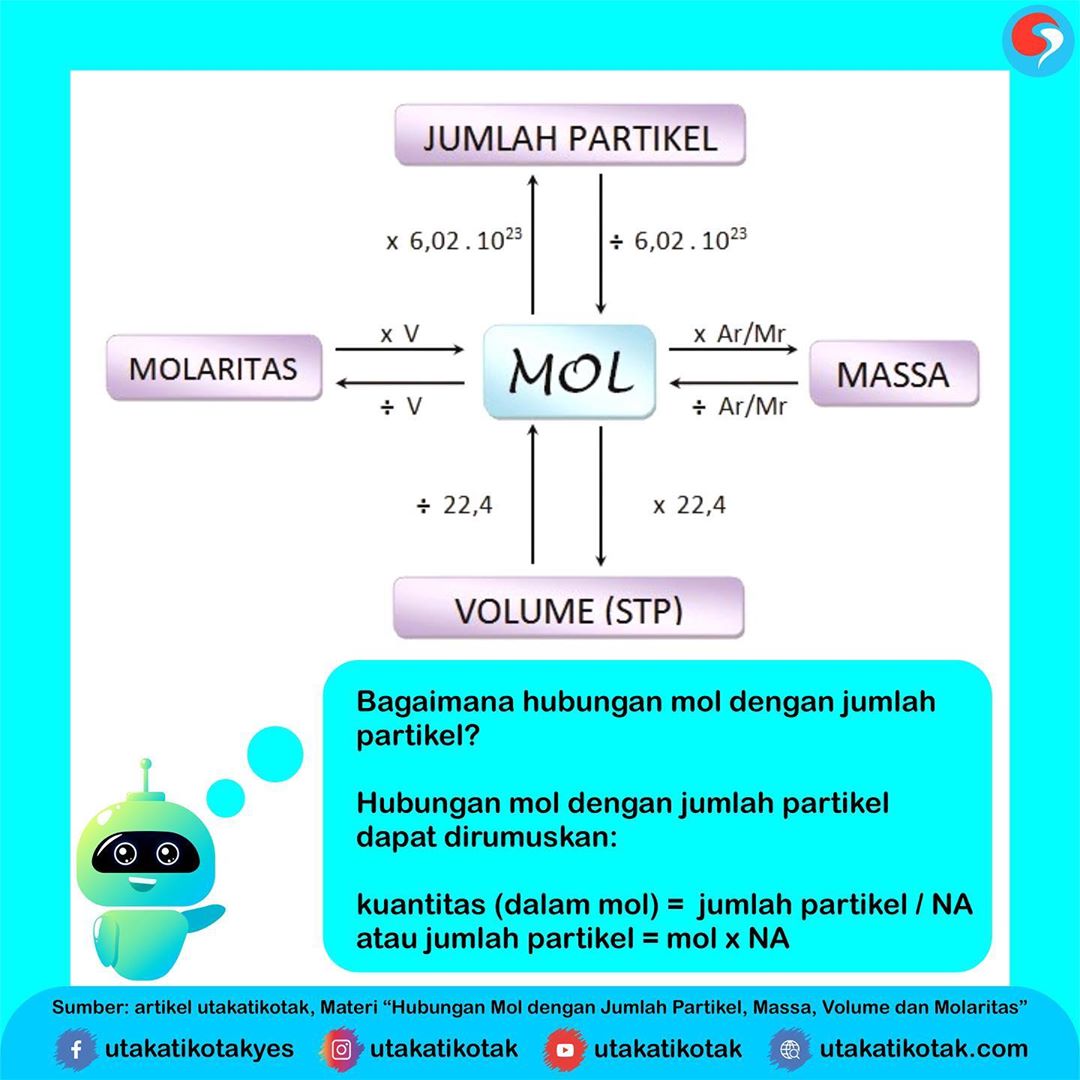
Hubungan Mol dengan Jumlah Partikel, Massa, Vo
Banyaknya partikel dinyatakan dalam satuan mol. Satuan mol sekarang dinyatakan sebagai jumlah partikel (atom, molekul, atau ion) dalam suatu zat. Para ahli sepakat bahwa satu mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12,0 gram isotop C -12 yakni 6,02 x 10 23 partikel.
Perhatikan grafik berikut! Jika jumlah mol partikel pelar...
Dalam bidang kimia ada beberapa satuan yang sering digunakan untuk menyatakan konsentrasi larutan ( banyaknya zat terlarut dalam sejumlah pelarut ). Beberapa satuan konsentrasi itu antara lain : mol, molalitas, molaritas, normalitas, ppm, persen massa, persen volum. Berikut akan saya jelaskan pengertian dan rumus dari satuan-satuan di atas : 1.

Fraksi mol dan molalitas (m) Soal dan Pembahasan KIMIA KELAS 12 YouTube
Konsep Mol Mol adalah satuan dasar SI (Satuan Internasional) yang mengukur jumlah zat. Jika Anda telah mempelajari atom, molekul dan ion sebagai partikel-partikel materi. Bagaimana caranya menghitung jumlah yang sangat banyak dari partikel-partikel materi yang berukuran sangat kecil tersebut? Untuk menyederhanakan jumlah partikel yang sangat kecil ini digunakan istilah MOL.