Konfigurasi Elektron Istilah, Konsep, Aturan, Penulisan InformasainsEdu
Konfigurasi ini dapat memberikan petunjuk yang berharga mengenai perilaku atom dalam berbagai reaksi kimia. Nah, dalam artikel ini, kita akan menjelajahi konfigurasi elektron berdasarkan subkulit dengan gaya santai yang akan membuatmu semakin peka terhadap keajaiban dunia kecil di sekitar kita.

Konfigurasi Elektron dengan Metode Subkulit YouTube
Konfigurasi elektron adalah suatu cara penulisan yang menunjukkan distribusi elektron dalam orbital-orbital pada kulit utama dan subkulit. Pada penulisan konfigurasi elektron perlu mempertimbangkan tiga aturan yaitu prinsip Aufbau, asas larangan Pauli dan kaidah Hund. Prinsip Aufbau Elektron-elektron dalam suatu atom berusaha menempati subkulit-subkulit yang berenergi rendah, kemudian baru ke.

Konfigurasi Elektron Subkulit Atom Swasti ll Belajar Kimia Online ll Kimia Kelas 10 YouTube
Dalam kurikulum KTSP, konfigurasi elektron berdasarkan kulit atom dipelajari di kelas X, sedangkan konfigurasi elektron berdasarkan subkulit dipelajari di kelas XI. Jumlah elektron maksimum yang bisa ditampung oleh kulit atom adalah 2n², dimana n adalah kulit ke-n. Kulit ke-1 dinamakan kulit K, kulit ke-2 dinamakan kulit L, dan seterusnya.

Konfigurasi Elektron subkulit YouTube
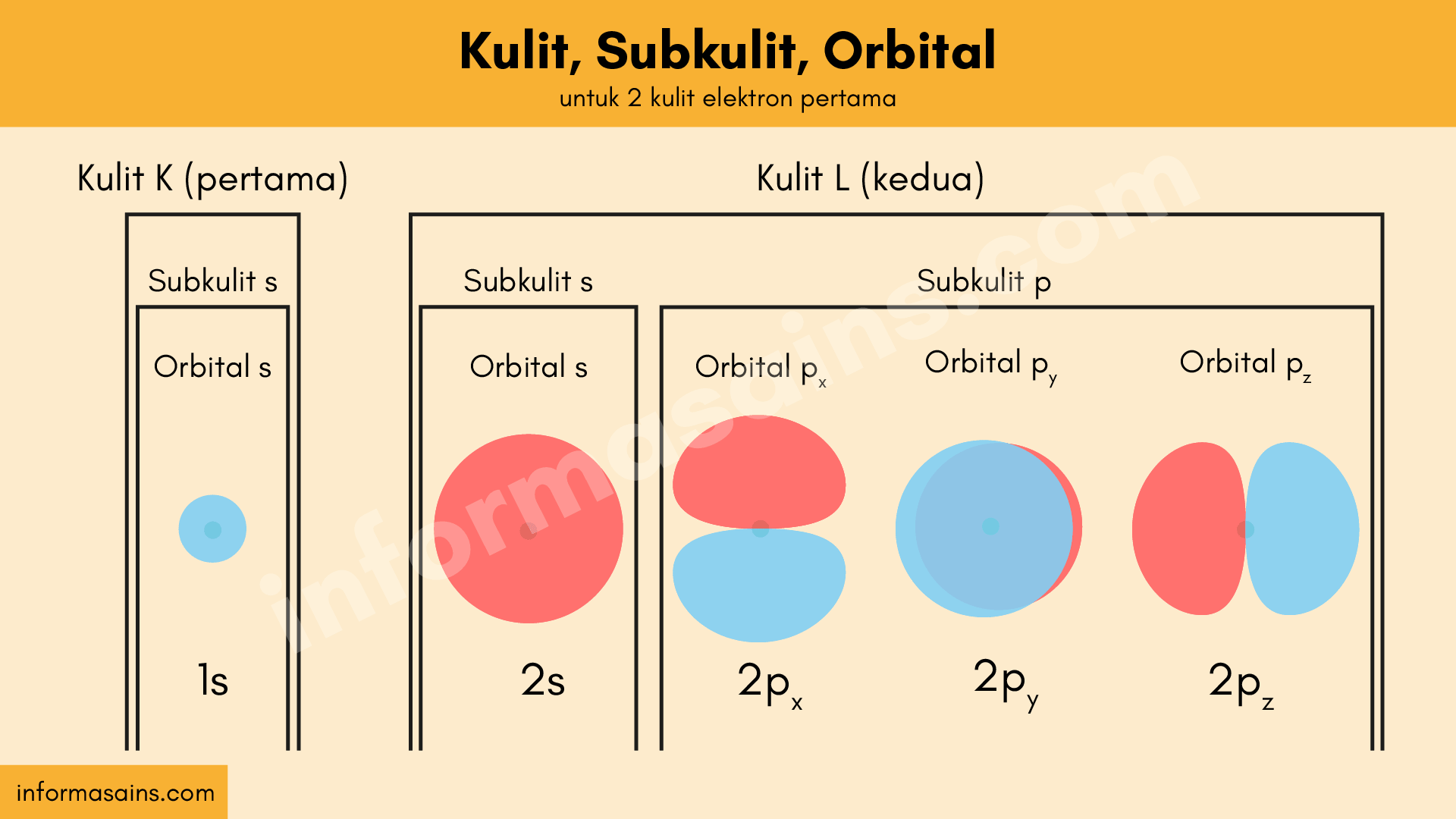
Pengertian Konfigurasi Elektron. Konfigurasi elektron adalah susunan elektron pada subkulit atom dalam orbital atom atau molekulnya. Harus diingat bahwa masing-masing orbital memiliki batas elektron yang dapat mengisinya. Berikut penjelasannya. Orbital s mampu diisi 2 elektron. Orbital p mampu diisi 6 elektron.

Konfigurasi Elektron dan Elektron Valensi
Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron $2n^{2}$, di mana n menunjukkan kulit atom. Contoh: $_{11}Na$: 2, 8, 1. Penulisan konfigurasi dengan cara ini memiliki keterbatasan yaitu hanya berlaku untuk unsur-unsur golongan logam utama. 2. Berdasarkan Konfigurasi Elektron Subkulit. a. Prinsip Aufbau

Tuliskan konfigurasi elektron subkulit, kemudian tentukan...
Berdasarkan Aturan Aufbau, konfigurasi elektron ini ditulis berdasarkan urutan tertentu sesuai dengan tingkat energi subkulit. Untuk menuliskan konfigurasi elektron, biasanya kita menggunakan diagram seperti pada gambar di atas untuk mengingat urutannya. Akan tetapi, metode ini saya rasa cukup ribet dan tidak efisien.

Soal Konfigurasi Elektron Subkulit Serta Menentukan Golongan dan Periode YouTube
Pengecualian Konfigurasi Elektron dalam Subkulit d dan f. Kestabilan suatu orbital dipengaruhi oleh sifat orbitalnya. Elektron dalam subkulit d akan lebih stabil apabila subkulit d berisi elektron penuh atau setengah penuh. Untuk mencapai kestabilan, satu elektron valensi dari subkulit s berpindah ke subkulit d. Penyimpangan juga terjadi pada.

Soal Konfigurasi Elektron subkulit part1 YouTube
Subkulit s = 1 kotak Subkulit p = 3 kotak Subkulit d = 5 kotak Subkulit f = 7 kotak. Dalam model mekanika kuantum, penulisan konfigurasi elektron menggunakan diagram orbital perlu mengikuti aturan penentuan konfigurasi elektron berdasarkan orbital. Kedudukan elektron terluar dari suatu atom bisa ditentukan melalui bilangan kuantumnya.
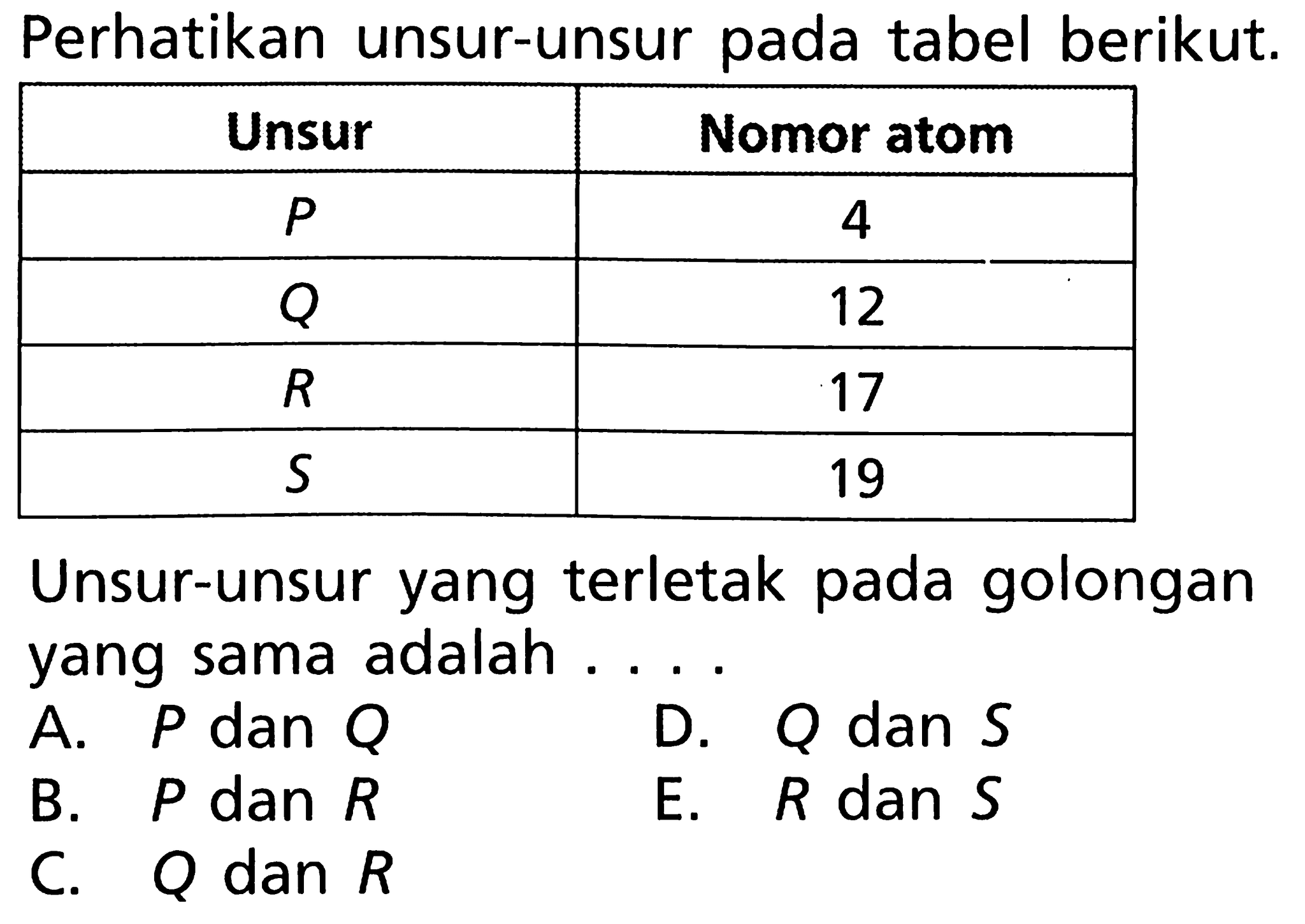
Tuliskan konfigurasi elektron subkulit, kemudian tentukan...
Dalam konfigurasi elektron subkulit, setiap kulit atom terdiri atas subkulit yang berisi bilangan kuantum atau kumpulan orbital s, p, d, dan f. Untuk lebih memudahkan penentuan nilai bilangan kuantum digunakan diagram orbital yang dilambangkan dengan sebuah kotak, yaitu: Subkulit s = 1 kotak; Subkulit p = 3 kotak; Subkulit d = 5 kotak; Subkulit.

Konfigurasi elektron suatu unsur berakhir pada subkulit
60 Contoh Konfigurasi Elektron Atom/Unsur berdasarkan Kulit, Subkulit, dan Gas Mulia. Perhatikan contoh konfigurasi elektron atom/unsur berdasarkan kulit, subkulit, dan gas mulia yang telah kami susun dalam bentuk tabel. 1. Tabel Contoh Konfigurasi Elektron Atom/Unsur berdasarkan Kulit. 2.

Konfigurasi Ion Berdasarkan Subkulit Atom YouTube
Konfigurasi elektron. Konfigurasi elektron atom gas netral dalam keadaan dasar. Disajikan berdasarkan subkulit dalam bentuk ringkas, dengan subkulit ditulis, dan dengan jumlah elektron per kulit. Konfigurasi elektron setelah unsur nobelium (unsur 102) adalah tentatif dan setelah rutherfordium (unsur 104) adalah prediksi.

SOAL UTBK [SBMPTN] KONFIGURASI ELEKTRON ION BERDASARKAN SUBKULIT DENGAN MUDAH YouTube
Playlist Konfigurasi Elektronhttps://www.youtube.com/watch?v=o3z3VuKuVnI&list=PLQ_4a1thWasOIfyThXfE8rLygP8tQ1Q9pJika teman-teman membutuhkan soal-soal latiha.

Cara Menentukan Jumlah Pasangan Elektron Pada Konfigurasi Subkulit YouTube
Konfigurasi elektron adalah penataan elektron dari suatu atom ke dalam kulit dan subkulit atom. Konfigurasi elektron ditulis berdasarkan Aturan Aufbau.Menurut Aturan Aufbau, konfigurasi elektron dimulai dari subkulit dengan tingkat energi paling rendah, diikuti subkulit dengan energi yang setingkat lebih tinggi, sampai semua elektron tersebar dalam subkulit atom.

KONFIGURASI ELEKTRONBerdasarkan Orbital( Subkulit ) Kelas 10 Materikimia
Nah sekarang kita akan menggambarkan konfigurasi elektron memakai diagram orbital, teman. Sebenarnya gambarnya cukup mudah kok. Suatu subkulit punya sejumlah orbital. Orbital itu digambarkan sebagai persegi dan berisi garis setengah panah yang mewakili elektron. Subkulit s punya 1 orbital, p punya 3 orbital, d punya 5 orbital, dan f 14 orbital.

Kimia Konfigurasi Elektron Subkulit (Aturan Aufbau) YouTube
Cara Menentukan Konfigurasi Elektron. Source: Thecityfoundry.com. Pada dasarnya, konfigurasi elektron adalah urutan angka yang menunjukkan letak elektron pada atom. Seperti yang telah kita ketahui, atom terdiri dari inti yang berisi proton dan neutron, serta lapisan elektron di sekelilingnya.

pembahasan soal kimia notasi atom dan konfigurasi subkulit YouTube
Konfigurasi dari atom O adalah 2 6, konfigurasi atom Ca adalah 2 8 8 2 dan konfigurasi atom Kr adalah 2 8 18 8 Konfigurasi elektron pada kulit atom juga berkaitan dengan adanya kation dan anion. Kation merupakan ion positif yang melepaskan elektron sedangkan, anion merupakan ion negative yang menyerap atau menerima elektron.