
Memahami Konfigurasi Elektron dan Diagram Orbital Lebih Mudah Kimia Kelas 10
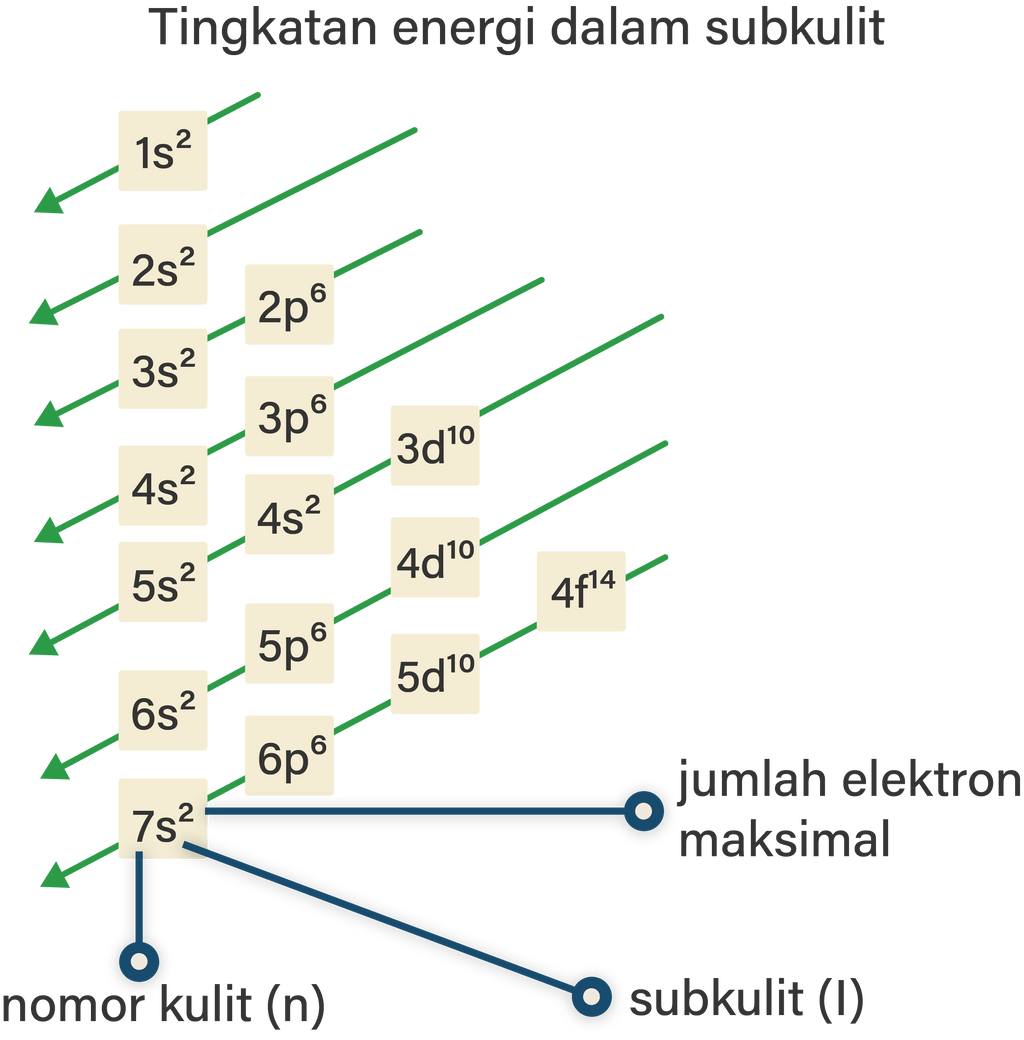
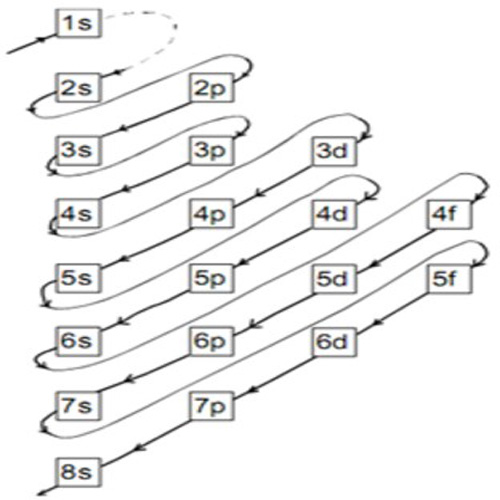
Jumlah elektron maksimal yang menempati subkulit atom adalah 2 untuk subkulit s, 6 untuk subkulit p, 10 untuk subkulit d, dan 14 untuk subkulit f. Sehingga lebih lengkapnya, konfigurasi elektron mengikuti urutan berikut. 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6 7s 2 5f 14 6d 10 7p 6. Contoh: 16 S : 1s 2 2s.
Jelaskan tentang konfigurasi elektron beserta cont...
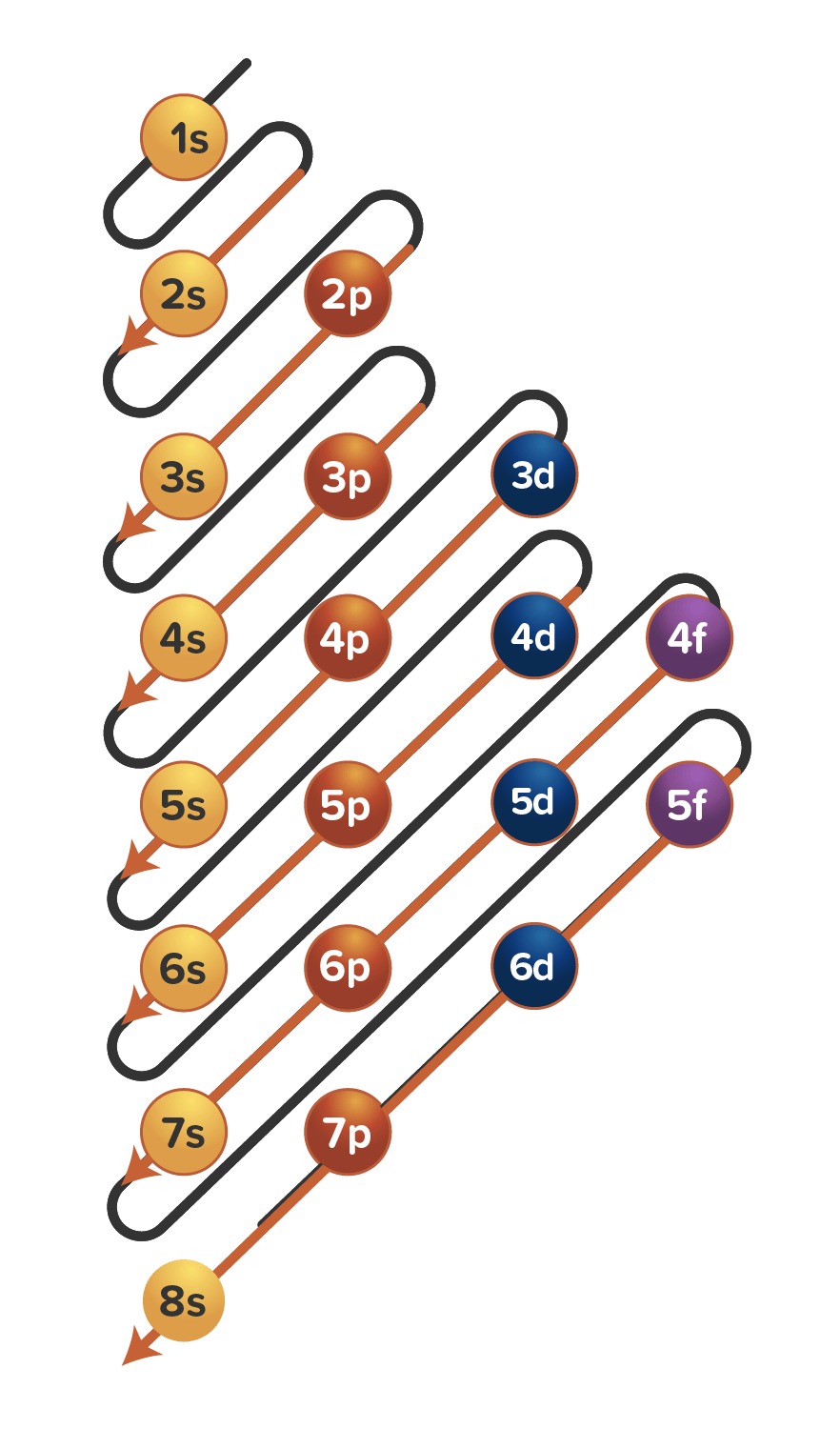
Pada gambar terlihat bahwa konfigurasi elektron dengan Prinsip Aufbau bergantung pada penjumlahan bilangan kuantum utama (n) dan bilangan kuantum azimuth (l). Urutan energi orbital atom dari yang paling rendah ke yang paling tinggi adalah 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, dan seterusnya.

Konfigurasi Elektron dalam Tabel Periodik (Kimia SBMPTN, UN, SMA) YouTube
Oleh karena itu, susunan elektron valensi suatu unsur sangat mempengaruhi atau merupakan penentu sifat-sifat kimia suatu atom. Unsur-unsur yang m. Contoh Soal. Tentukan elektron valensi dari Natrium (Na)! Jawaban: Nomor atom (Z) Natrium (Na) adalah 11, maka (Na) = 2. 8. 1. Sehingga. Jumlah kulit Na = 3. Kulit terluar Na = M. Elektron valensi = 1

Konfigurasi elektron unsur R yang paling sesuai adalah....
Teori Atom Bohr. Lintasan-lintasan elektron disebut juga dengan kulit elektron, yang ditempati oleh jumlah elektron maksimal. Dalam teori ini, konfigurasi elektron adalah pengisian elektron yang dimulai dari tingkat energi (kulit) paling rendah, yaitu kulit yang pertama kulit K, setelah kulit K sudah terisi penuh, dilanjutkan ke kulit L, kulit M, kulit N, hingga seterusnya.
Tuliskan konfigurasi elektronnya dan tentukan pula...
Contoh soal Konfigurasi Elektron. Tentukan konfigurasi elektron dari 20Ca! Jawab: Ca memiliki jumlah elektron 20, maka konfigurasinya adalah: 1s2 2s2 2p6 3s2 3p6 4s2 Aturan Penuh/Setengah Penuh. Aturan penuh dan setengah penuh pada konfigurasi elektron menyatakan bahwa suatu elektron dapat berpindah ke orbital lain untuk mencapai susunan yang.
Konfigurasi Elektron Menurut Larangan Pauli Rumus Kimia
Tabel konfigurasi elektron. Konfigurasi elektron adalah susunan elektron-elektron yang terdapat pada suatu unsur. Konfigurasi elektron dituliskan berdasarkan aturan yang telah disepakati oleh ilmuan-ilmuan terkemuka. Aturan-aturan dalam penulisan konfigurasi elektron antara lain yaitu prinsip aufbau, kaidah hund, larangan pauli, serta hukum mekanika kuantum.

Cara menulis konfigurasi elektron dan mengisi diagram orbital YouTube
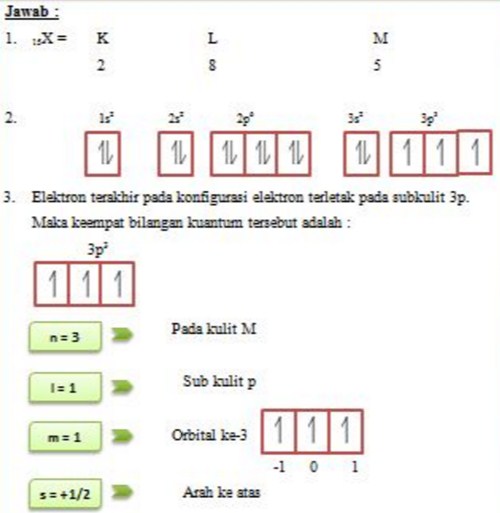
Nah sekarang kita akan menggambarkan konfigurasi elektron memakai diagram orbital, teman. Sebenarnya gambarnya cukup mudah kok. Suatu subkulit punya sejumlah orbital. Orbital itu digambarkan sebagai persegi dan berisi garis setengah panah yang mewakili elektron. Subkulit s punya 1 orbital, p punya 3 orbital, d punya 5 orbital, dan f 14 orbital.

Konfigurasi Elektron Ion Panduan Lengkap dan Terperinci
Konfigurasi elektron adalah susunan penyebaran (pengisian). Diagram orbital dan konfigurasi elektron berdasarkan orbital dari 10 unsur pertama (Sumber: Gilbert, Thomas N.et al. 2012. Chemistry:. terdapat anomali konfigurasi elektron dari aturan-aturan di atas. Subkulit d memiliki tendensi untuk terisi setengah penuh atau terisi penuh.

Aturan Konfigurasi Elektron Dan Diagram Orbital Superprof
Untuk mempermudah penentuan konfigurasi elektron, gunakan Hukum Pauli, yang menyatakan bahwa elektron-elektron memiliki nilai spin, yaitu +1/2 atau -1/2. Proses penentuan konfigurasi elektron terdiri dari beberapa langkah. Langkah pertama adalah pengurutan unsur berdasarkan nomor atomnya dengan cara meningkatkan nilainya. Hal ini penting untuk.

Pengertian Konfigurasi Elektron Ilmu Kimia
Konfigurasi elektron adalah suatu susunan penyebaran (pengisian) elektron-elektron dalam . Berikut langkah konfigurasi elektron berbagai atom. Disclaimer;. Berikut ini adalah konfigurasi elektron dari unsur gas mulia. 2 He = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6; 10 Ne = 1s 2 2s 2 2p 6;

Konfigurasi Elektron Berdasarkan Orbital YouTube
Konfigurasi elektron. Konfigurasi elektron atom gas netral dalam keadaan dasar. Disajikan berdasarkan subkulit dalam bentuk ringkas, dengan subkulit ditulis, dan dengan jumlah elektron per kulit. Konfigurasi elektron setelah unsur nobelium (unsur 102) adalah tentatif dan setelah rutherfordium (unsur 104) adalah prediksi.

Konfigurasi Elektron
Konfigurasi elektron adalah susunan elektron pada subkulit atom dalam orbital atom atau molekulnya. Pelajari Pengertian Aturan Gas Mulia Contoh Soal.. Berikut ini adalah konfigurasi elektron dari unsur gas mulia. 2 He = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6. 10 Ne = 1s 2 2s 2 2p 6.
Pengertian Konfigurasi Elektron Rumus Kimia
Konfigurasi elektron dari atom Cl adalah 1s 2 2s 2 2p 6 3s 2 3p 5, maka konfigurasi elektron dari ion Cl - adalah 1s 2 2s 2 2p 6 3s 2 3p 6 (satu elektron telah diterima dan masuk ke kulit terluar di subkulit 3p) Contoh Soal. Tuliskanlah konfigurasi elektron dari unsur - unsur berikut ini tanpa menggunakan penyingkatan. a) 37 Rb b) 32 Ge c.
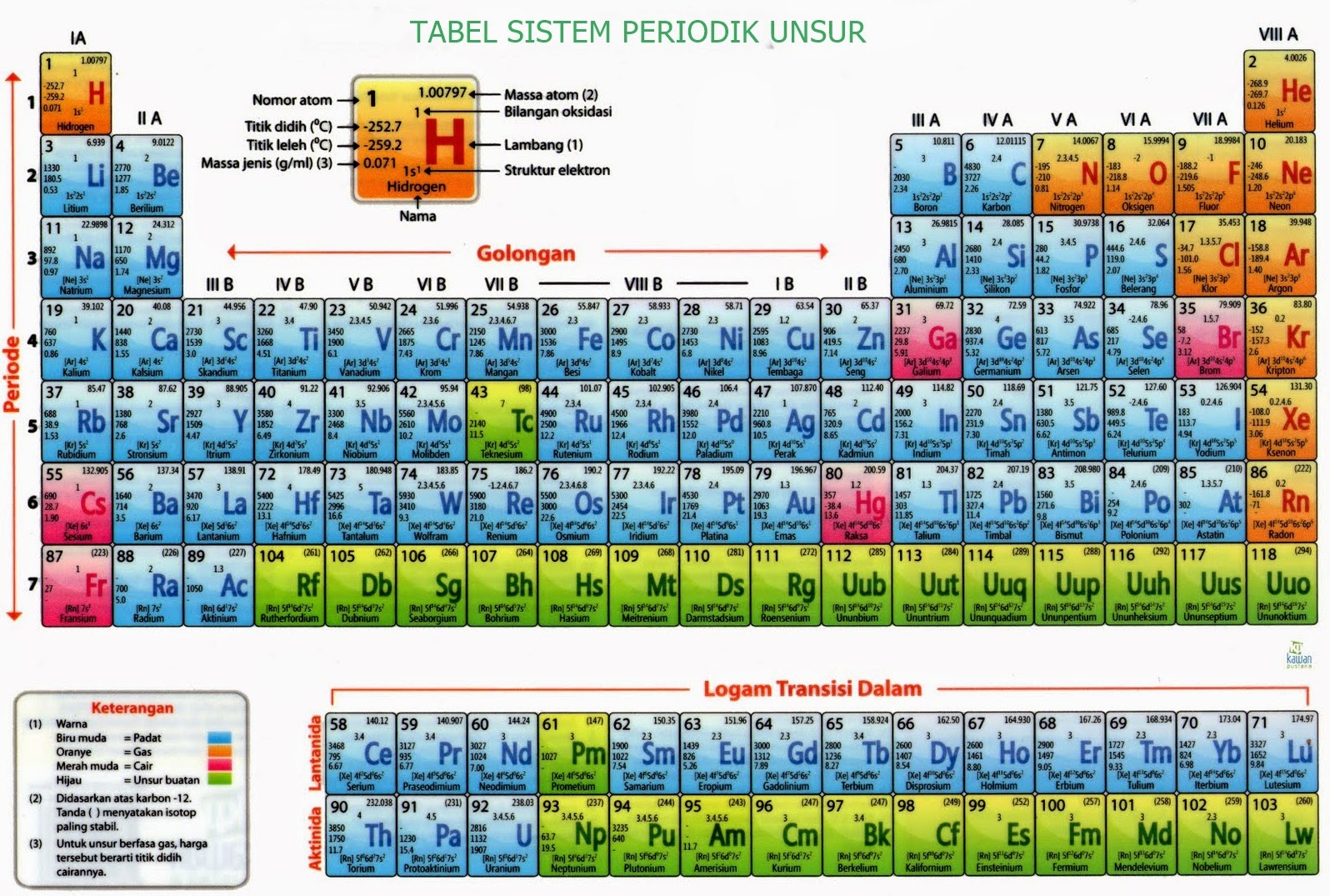
Tabel Sistem Periodik Unsur dan Penjelasannya Lengkap
Banyaknya jumlah elektron terluar (elektron valensi) dari suatu atom menentukan sifat-sifat kimia suatu unsur. Konfigurasi elektron dapat dituliskan dengan cara: 1. Berdasarkan Kulit. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2n2 2 n 2, di mana n menunjukkan kulit atom. Contoh: 11Na 11 N a: 2, 8, 1.

Konfigurasi Elektron dan Elektron Valensi
Penentuan konfigurasi elektron cara per kulit didasari oleh jumlah elektron yang dapat mengisi setiap kulit. Jumlah maksimum elektron yang dapat mengisi setiap kulit dirumuskan dengan 2n² (n= kulit yang ditempati elektron). Jumlah elektron secara maksimal yang dapat ditempati pada setiap kulit yaitu kulit pertama (kulit K) memiliki 2 elektron.

Perhatikan konfigurasi elektron unsur dan Y berikut! Jika...
Untuk contoh lainnya, bisa dicoba unsur lainnya. Misalnya unsur Cl atau chlorin. Unsur ini memiliki elektron sebesar 17. Maka konfigurasi elektronnya adalah 1s2 2s2 2p6 3s2 3p5. Bisa Anda buktikan dengan menjumlah elektronnya yaitu 2+2+6+2+5 = 17. Dari pemahaman seperti ini, Anda bisa terus berlatih dan mencoba berbagai macam unsur lainnya.