Jelaskan tentang konfigurasi elektron beserta cont...
Banyaknya jumlah elektron terluar (elektron valensi) dari suatu atom menentukan sifat-sifat kimia suatu unsur. Konfigurasi elektron dapat dituliskan dengan cara: 1. Berdasarkan Kulit. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2n2 2 n 2, di mana n menunjukkan kulit atom. Contoh: 11Na 11 N a: 2, 8, 1.
Konfigurasi Elektron Pengertian, Cara Menentukan, & Contoh Soal
Konfigurasi Elektron: Cr (Z = 24): [Ar] 4s 1 3d 5: Cu (Z = 29): [Ar] 4s 1 3d 10: Konfigurasi elektron adalah. Konfigurasi elektron adalah susunan elektron-elektron pada sebuah atom, molekul, atau struktur fisik lainnya. Sama seperti partikel elementer lainnya, elektron patuh pada hukum mekanika kuantum dan menampilkan sifat-sifat bak-partikel.
Tentukan konfigurasi elektron dari atom berikut!
Bisakimia akan mencoba memberikanRangkuman Konfigurasi Elektron Paling lengkap yang disusun secara sitematis dan jelas. Walaupun sebelumnya telah banyak juga materi Kimia SMA di bisa kimia , yaitu pada artikel : Aturan Aufbau pada Konfigurasi Elektron. Mempelajari menentukan konfigurasi elektron dengan mudah yuk.

Memahami Konfigurasi Elektron dan Diagram Orbital Lebih Mudah Kimia Kelas 10
Konfigurasi Elektron. Selamat Datang dan Selamat Belajar di Wardaya College! Di sini, kamu akan belajar tentang Konfigurasi Elektron melalui latihan soal interaktif dalam 3 tingkat kesulitan (mudah, sedang, sukar). Apabila materi ini berguna, bagikan ke teman atau rekan kamu supaya mereka juga mendapatkan manfaatnya.

Konfigurasi Elektron dan Elektron Valensi
Tuliskan konfigurasi elektron gas mulia He, Ne, Ar, Kr, Xe, Ra dan tentukan elektron valensi! Jawaban: Konfigurasi elektron gas mulia adalah: Unsur gas mulia adalah: 1. Helium (He), nomor atom 2, konfigurasi elektron: 2 atau "1s2" 2. Neon (Ne), nomor atom 10, konfigurasi elektron: 2, 8 atau "1s2; 2s2 2p6" 3.

Pengertian Konfigurasi Elektron Ilmu Kimia
Penulisan konfigurasi elektron dapat secara panjang (sesuai aturan Aufbau) dan dapat secara singkat. Contoh penulisan konfigurasi elektron secara singkat yang didasarkan pada konfigurasai gas mulia yaitu seperti pada tabel berikut.. Konfigurasi Elektron Stabil; Cr: 24 [Ar] 4s 2 3d 4 [Ar] 4s 1 3d 5: Cu: 29 [Ar] 4s 2 3d 9 [Ar] 4s 1 3d 10: Mo.

Ion Berikut Yang Mempunyai Konfigurasi Elektron Ar 3d 4 Adalah bukan merupakan tujuan evaluasi
Dalam fisika atom dan kimia kuantum, konfigurasi elektron adalah susunan elektron-elektron pada sebuah atom, molekul, atau struktur fisik lainnya.. Kalium dan kalsium muncul dalam tabel periodik sebelum logam transisi, dan memiliki konfigurasi elektron [Ar] 4s 1 dan [Ar] 4s 2 (orbital 4s diisi terlebih dahulu sebelum orbital 3d).

Contoh Soal Konfigurasi Elektron Beserta Pembahasannya
Argon (Ar) Gas mulia selanjutnya adalah argon yang memiliki nomor atom 18. 18 elektron argon mengisi 3 kulit elektron dengan konfigurasi sebagai berikut: Terlihat di kulit valensi (kulit ketiga) terdapat 8 elektron yang lagi-lagi memenuhi aturan oktet. Baca juga: Aturan Oktet dalam Kimia.

Suatu unsur mempunyai konfigurasi elektron [Ar] 3d^10 4s^...
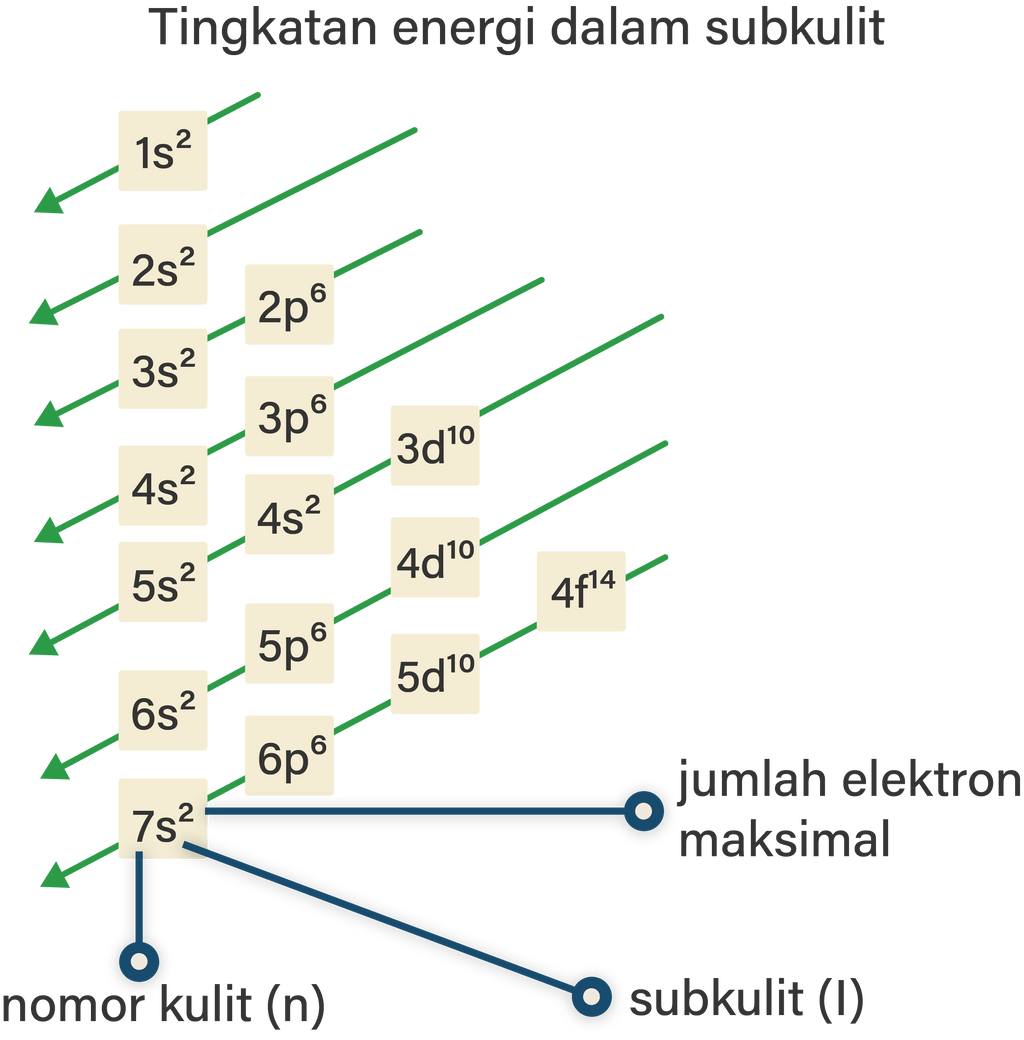
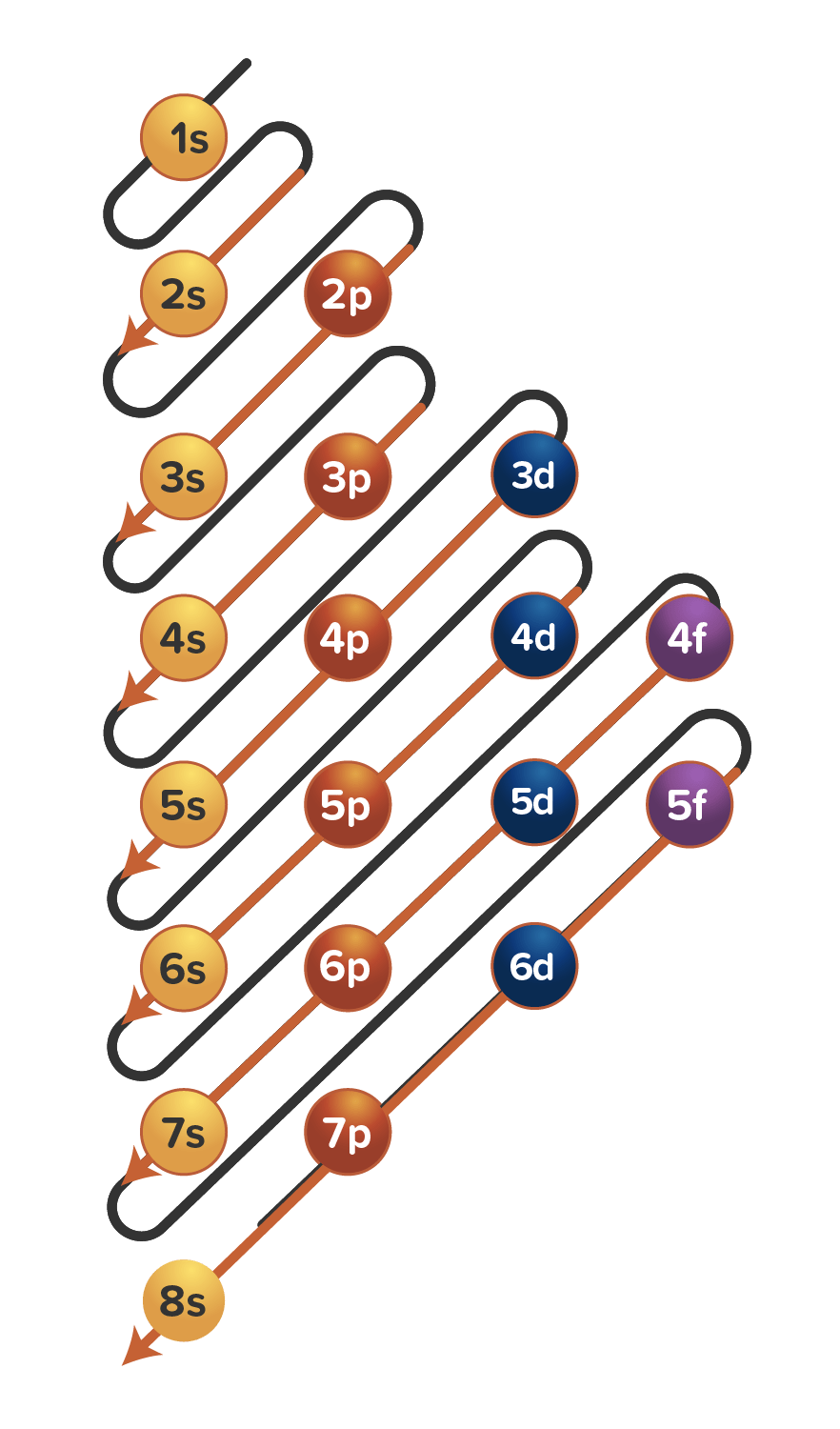
Aturan penentuan konfigurasi elektron berdasarkan orbital: 1. Asas Aufbau: Elektron menempati orbital-orbital dimulai dari tingkat energi yang terendah, dimulai dari 1s, 2s, 2p, dan seterusnya seperti urutan subkulit yang terlihat pada Gambar 2. Gambar 2. Urutan tingkat energi subkulit.

Aturan Konfigurasi Elektron Dan Diagram Orbital Superprof
34 Se: [Ar] 4s 2 3d 10 4p 4 . Tabel konfigurasi elektron dari unsur - unsur dengan nomor atom 1 sampai 20. Nomor Atom. Nama Unsur: Simbol: Konfigurasi Elektron. 1: Hidrogen: H: 1s 1: 2: Helium: He: 1s 2: 3: Litium: Li [He] 2s 1: 4:. Konfigurasi Elektron Ion. Ion adalah atom atau molekul yang memiliki muatan. Terdapat dua jenis ion yaitu.

Tulis dan gambarkan konfigurasi elektron dari atom atom...
Konfigurasi elektron Ar dapat disingkat menjadi, Ar = [Ne] 3s 2 3p 6. Na = 1s 2 2s 2 2p 6 3s 1, dapat disingkat. Na = [Ne] 3s 1. Baca juga: Sifat Unsur Halogen dan Manfaatnya dalam Kehidupan Sehari-hari . Macam-macam Gas Mulia. Seperti yang sudah disebutkan sebelumnya, unsur-unsur gas mulia terdiri dari 6 unsur, yaitu helium, neon, argon.

Penjelasan Konfigurasi Elektron Secara Lengkap
Konfigurasi elektron adalah susunan elektron pada subkulit atom dalam orbital atom atau molekulnya. Pelajari Pengertian Aturan Gas Mulia Contoh Soal. Langsung ke isi. Search. Kimia; Matematika; Fisika;. 18 Ar = 1s 2 2s 2 2p 6 3s 2 3p 6 . 36 Kr = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6.

Konfigurasi elektron atom Fe [Ar] 3d6 4s2. Jumlah elektron yg tidak berpasangan pada atom Fe
Konfigurasi elektron gas mulia digunakan untuk menyederhanakan atau meringkas konfigurasi elektron unsur yang lain. Misalnya konfigurasi elektron atom Mn adalah 1s2 2s2 2p6 3s2 3p6 4s2 3d5, jika disederhanakan dapat ditulis 25Mn [Ar] 4s2 3d5 atau 25Mn [Ar] 3d5 4s2.

Jika unsur dengan konfigurasi elektron [Ar] 4s^2 3d^10 ak...
Konfigurasi elektron. Konfigurasi elektron atom gas netral dalam keadaan dasar. Disajikan berdasarkan subkulit dalam bentuk ringkas, dengan subkulit ditulis, dan dengan jumlah elektron per kulit. Konfigurasi elektron. 18 Ar argon: [Ne] 3s 2 3p 6; 1s 2: 2s 2: 2p 6: 3s 2: 3p 6: 2: 8: 8: 19 K kalium: [Ar] 4s 1; 1s 2: 2s 2: 2p 6: 3s 2: 3p 6: 4s.

KONFIGURASI ELEKTRON TEORI ATOM BOHR YouTube
Tabel konfigurasi elektron. Konfigurasi elektron adalah susunan elektron-elektron yang terdapat pada suatu unsur. Konfigurasi elektron dituliskan berdasarkan aturan yang telah disepakati oleh ilmuan-ilmuan terkemuka. Aturan-aturan dalam penulisan konfigurasi elektron antara lain yaitu prinsip aufbau, kaidah hund, larangan pauli, serta hukum mekanika kuantum.
Pengertian Konfigurasi Elektron Rumus Kimia
Konfigurasi elektron adalah suatu susunan penyebaran (pengisian) elektron-elektron dalam . Berikut langkah konfigurasi elektron berbagai atom.. (Z = 28) maka konfigurasinya adalah 1s2 2s2 2p6 3s2 3p6 4s2 3d8 atau [Ar] 4s2 3d8 dan jumlah elektron pada setiap kulit adalah K berjumlah 2, L berjumlah 8, M berjumlah 16 dan N berjumlah 2Sr (Z = 38.