
apa perbedaan molalitas dan molaritas Brainly.co.id
Hitung molalitas dan fraksi mol larutan KOH dalam air yang kadarnya 28% (Mr KOH = 56) Satuan Konsentrasi Larutan; Sifat Koligatif Larutan;. n p sebesar sehingga menjadi 0,5 per 4,5 diperoleh nilai x t sebesar 0,11 maka Kesimpulannya adalah sebesar 6,94 molal dan nilai fraksi mol dari larutan KOH atau XT sebesar 0,1 Oke sampai juga di soal.

Hitunglah molalitas dan fraksi mol larutan NaOH dalam air yang kadarnya 40 (Mr NaOH = 40
Ingat, rumus molaritas pencampuran adalah: Maka, konsentrasi larutan setelah dicampurkan adalah: M campuran = (100 x 0,1) + (150 x 0,2) / (100 + 150) = 40 / 250. = 0,16 M. Quipperian, itu dia pembahasan mengenai rumus molaritas beserta contoh soal dan pembahasannya. Agar semakin paham dan mahir dalam menggunakan rumus molaritas, cobalah untuk.

Menghitung Molalitas, Molaritas, Fraksi Mol, dan Persen () Massa !! SIfat Koligatif Larutan
Konsentrasi Larutan: Pengantar, Persen Massa, Molaritas, Molalitas, Fraksi Mol [Lengkap+Contoh Soal] Ditulis oleh Husnul Khatimah • 17 Februari 2024. Banyaknya zat terlarut dalam larutan dinyatakan dengan konsentrasi larutan yang terdiri dari persen massa, molaritas, molalitas, dan fraksi mol. Pada artikel ini akan membahas materi konsentrasi.
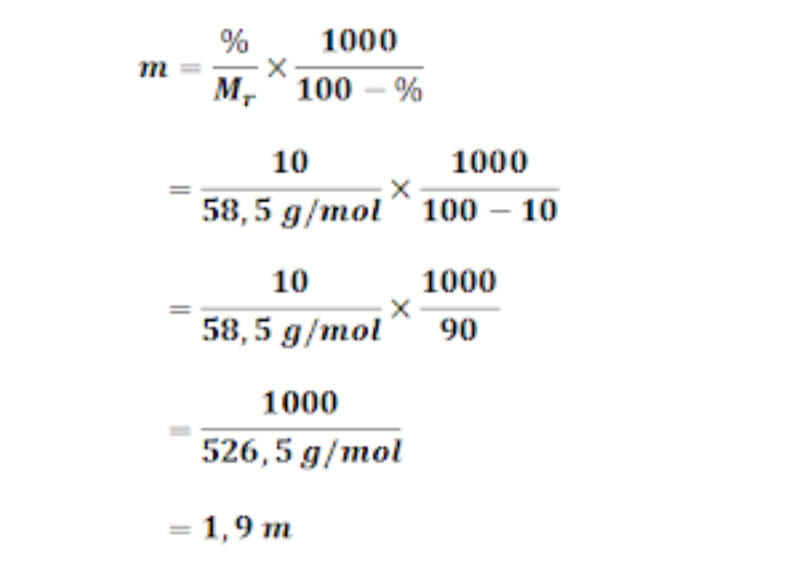
Cara Menghitung dan Contoh Soal Fraksi Mol dan Jawabannya Rumus dan Pembahasan Fraksi Mol
n = gram/Mr = 3/60 = 0,05 mol. Setelah diketahui molnya, kita bisa menggunakan rumus molaritas larutan urea. M = n/V = 0,05/0,25 = 0,2 Molar. Jadi, molaritas dari larutan urea adalah 0,2 Molar atau 0,2 mol/liter. Itu dia penjelasan mengenai rumus molaritas dan molalitas suatu larutan dalam Kimia. Masih sering merasa kesulitan belajar materi.

Materi Lengkap Molalitas Dan Fraksi Mol Beserta Contohnya Sains Seru Riset
Hitung molalitas dan fraksi mol larutan KOH dalam air yang kadarnya 28% (Mr KOH = 56)Hal 8 no 3 Kimia 3 Unggul Sudarmo Erlangga-----.

Contoh Soal Molalitas dan Fraksi Mol larutan LABORATORIUM SMK
menghitung jumlah mol dari 10 gram garam dapur (NaCl) yang diketahui mempunyai massa relatif molekul 58,5. Jumlah mol , n = gram/Mr = 10/58,5 = 0,171 mol. jumlah mol 10 gram garam dapur yaitu 0,171 mol. Contoh perhitungan molaritas larutan

Menghitung Molalitas Larutan Jika Diketahui Molaritas dan Kerapatan Larutannya YouTube
Pengertian Fraksi Mol. Fraksi mol adalah besaran konsentrasi larutan. Fraksi mol menyatakan perbandingan jumlah mol zat terlarut terhadap jumlah mol larutan. Fraksi mol tidak memiliki satuan, sehingga dinotasikan dengan X. Contohnya fraksi mol urea 01, ditulis dengan X urea 0,1. Artinya, larutan yang mengandung 0,1 bagian mol urea dalam 1.

Cara Menghitung Molaritas, Molalitas, dan Fraksi Mol YouTube
Hai CoFriends, yuk latihan soal ini:Hitung molalitas dan fraksi mol larutan KOH dalam air yang kadarnya 28% (Mr KOH = 56) Topik atau Materi: Satuan Konsentra.

fraksi mol natrium hidroksida(Mr 40)suatu larutan
Soal dan Jawaban Konsentrasi Larutan: Molaritas, Molalitas, Fraksi Mol, Persen Berat, Normalitas. 1. Konversi molal ke % massa. Contoh soal: Hitunglah % massa dari larutan NaI 0,2 molal (massa molar NaI = 150 g/mol) Penyelesaian: Arti 0,2 molal NaI adalah 0,2 mol NaI dalam 1 Kg pelarut air. massa NaI sebanyak 0,2 mol = 0,2 mol x 150 g/mol = 30.

Rumus Fraksi Mol Pengertian, Sifat dan Contoh Soalnya Lengkap BprsKu.Co.Id
Jelaskan perbedaan antara molaritas, molalitas dan normalitas, serta tuliskan rumusnya! Molaritas dari suatu solute adalah jumlah mol solute per liter larutan dan ditandai dengan huruf besar M. Molalitas dari suatu solute adalah jumlah mol solute per 1000gr solven. Molalitas ditulis dengan huruf kecil m.

Contoh Soal Molalitas Homecare24
Sebuah larutan terdiri dari 3 mol zat A, 3 mol zat B, dan 4 mol zat C. Hitung fraksi mol dari masing - masing zat tersebut ? Pembahasan : Diketahui: nA = 3; nB = 3; nC = 4; Penyelesaian:. Hitunglah molalitas dan fraksi mol larutan NaOH dalam air yang berkadar 40% (Mr NaOH = 40)! Pembahasan: Diketahui: Larutan air dengan kadar NaOH dengan.

Fraksi mol dan molalitas (m) Soal dan Pembahasan KIMIA KELAS 12 YouTube
Contoh Soal Fraksi Mol dan Pembahasannya. Nah, kalau elo udah ngerasa cukup menguasai materi ini baik dari segi definisi maupun rumusnya, mungkin kita udah bisa uji pemahaman elo lewat dua soal di bawah ini. 1. Suatu larutan, memiliki fraksi mol zat terlarut sebesar 0,2.

Contoh Soal Fraksi Mol Dan Pembahasannya
Rumus Molaritas. Molaritas termasuk konsentrasi larutan. Dari berbagai bentuk konsentrasi yang dipengaruhi sifat koligatif larutan yaitu molaritas, molalitas, dan fraksi mol. Satuan molaritas adalah mol/liter atau M. Rumus molaritas yaitu mol zat terlarut dibagi volume larutan. Tetapi, molaritas dapat dicari melalui massa jenis zat terlarut dan volume larutan.

Hitunglah molalitas dan fraksi mol larutan NaOH dalam air yang kadarnya 40 (Mr NaOH = 40
Dengan demikian, perbandingan fraksi mol KCl dan fraksi mol H 2 O adalah 0,2 : 0,8 = 1 : 4. Jadi, perbandingan fraksi mol KCl dan fraksi mol H 2 O adalah 1 : 4. Contoh Soal 3. Untuk membuat acar, Gilang melarutkan 60 gram cuka ke dalam 90 gram air. Tentukan fraksi mol cuka dan fraksi mol airnya! (Mr cuka = 60, Mr air = 18) Pembahasan: Diketahui.

Molalitas dan Fraksi Mol Larutan KOH no 3 hal 8 Erlangga YouTube
Satuan molalitas. Molalitas adalah besaran turunan yang memiliki satuan. Dilansir dari ChemistryGod, satuan standar molalitas adalah mol per kilogram (mol/kg) atau kerap disebut sebagai molal. Molal biasanya dilambangkan dengan huruf "m". Misalnya, molalitas suatu larutan adalah 12 mol/kg, maka dapat dinyatakan sebagai 12 molal atau 12 m.

Molaritas, Molalitas, dan Fraksi Mol (Part 2) 5NChemistry
3. 0.0. Jawaban terverifikasi. Hitung molalitas dan fraksi mol larutan KOH dalam air yang kadarnya 28% (Mr KOH= 56)