
20+ Contoh Soal Hidrolisis Asam Lemah Dan Basa Kuat Contoh Soal Terbaru
Daftar Nama Asam-Basa Kuat dan Asam-Basa Lemah. Skala pH yang menunjukan suatu larutan bersifat asam atau basa (lumenlearning.com) KOMPAS.com - Asam merupakan zat yang menghasilkan ion hidrogen (H+) dalam larutan. Sementara basa adalah zat yang menghasilkan ion hidroksida (OH-) dalam larutan. Asam dan basa dapat bereaksi menghasilkan air.
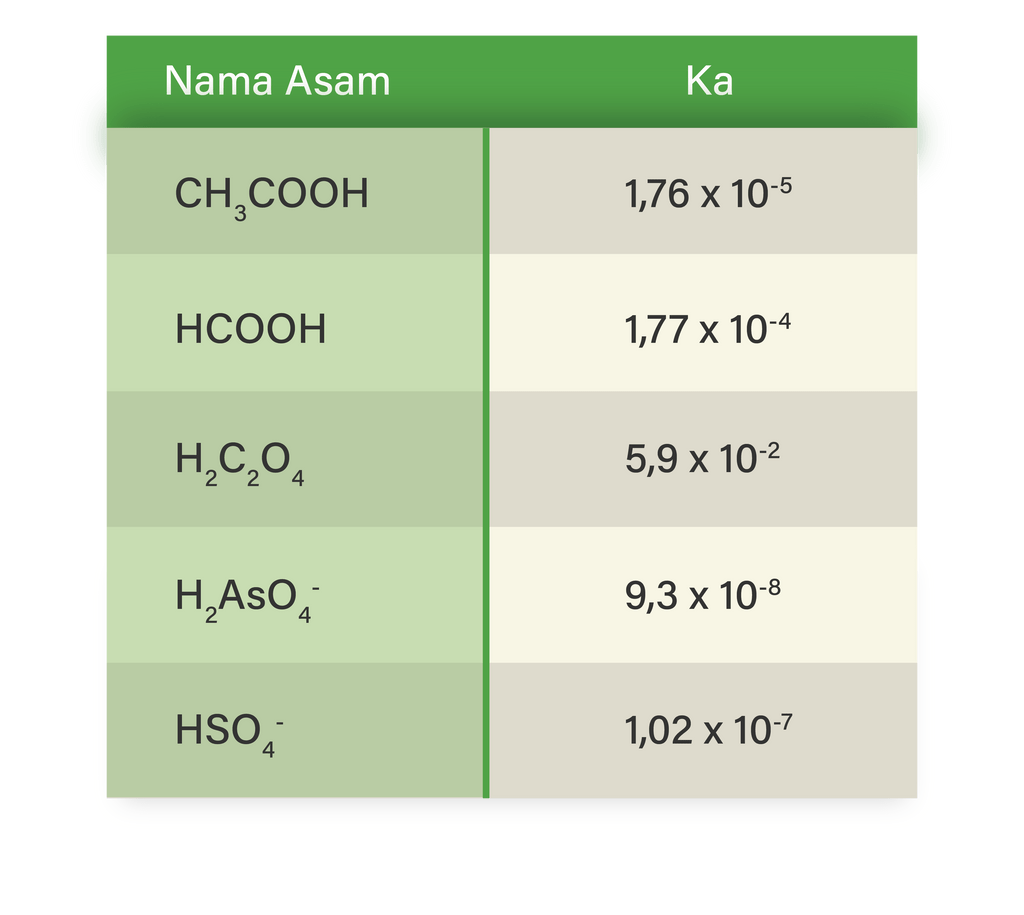
Diketahui nilai K a dari beberapa asam lemah ada...
Contoh asam kuat yaitu HCl, HNO 3, H 2 SO 4, dan HCIO 4. Sedangkan basa kuat adalah senyawa basa yang mudah melepaskan ion OH - dalam air dan mengalami disosiasi total dalam larutannya. Contoh basa kuat yaitu NaOH, KOH, dan Ba(OH) 2. 2. Asam Lemah dan Basa Lemah. Asam lemah adalah senyawa asam yang sulit melepaskan ion H + dalam air dan.

Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah
Kekuatan asam. Asam kuat. Asam lemah. Ringkasnya, asam sulfat (H 2 SO 4 ) adalah asam kuat yang hampir terdisosiasi sempurna menjadi ion hidrogen (H+) dan ion sulfat (SO 4 ) 2- dalam air. Ini menghasilkan konsentrasi ion H+ yang tinggi, menghasilkan pH yang sangat rendah dan sifat yang sangat korosif. Di sisi lain, asam lemah yang diwakili oleh.

Cara Menghitung Ph Asam Lemah Satu Manfaat
Artinya, perbedaan asam lemah dan asam kuat adalah asam kuat terdisosiasi sempurna dalam air, sedangkan asam lemah hanya terdisosiasi sebagian. Menurut Shikha Munjal dan Aakash Singh dalam The Arrhenius Acid and Base Theory (2020), asam kuat memiliki konsentrasi ion hydronium yang terbentuk sama dengan konsentrasi asam.

H2S Asam Atau Basa
1. Asam Kuat - Kekuatan Asam Kuat dan Asam Lemah. Asam kuat yaitu senyawa asam yang dalam larutannya terion seluruhnya menjadi ion-ionnya. Reaksi ionisasi asam kuat merupakan reaksi berkesudahan. Secara umum, ionisasi asam kuat dirumuskan sebagai berikut. HA(aq) → H+(aq) + A-(aq) Dengan: x = valensi asam. M = konsentrasi asam.

pH Campuran asam Lemah dan Asam KuatKimia SMA YouTube
Asam kuat dan asam lemah - Pengertian asam kuat adalah senyawa asam (biasanya asam anorganik) yang akan terionisasi dengan sempurna jika terlarut dalam air.. H atau C - O. Asam ini juga kerap dipakai untuk campuran bahan kosmetik. Contoh senyawa asam organik adalah: Asam asetat : cuka Asam askorbat : vitamin C Asam benzoat : pengawet makanan
Daftar Asam Basa Kuat Dan Lemah
Asam Lemah. Asam lemah tidak sepenuhnya terdisosiasi menjadi ion-ionnya dalam air. Sebagai contoh, HF berdisosiasi menjadi ion H + dan F - dalam air, tetapi beberapa HF tetap berada dalam larutan, sehingga bukan merupakan asam kuat. Ada lebih banyak asam lemah daripada asam kuat. Sebagian besar asam organik adalah asam lemah.
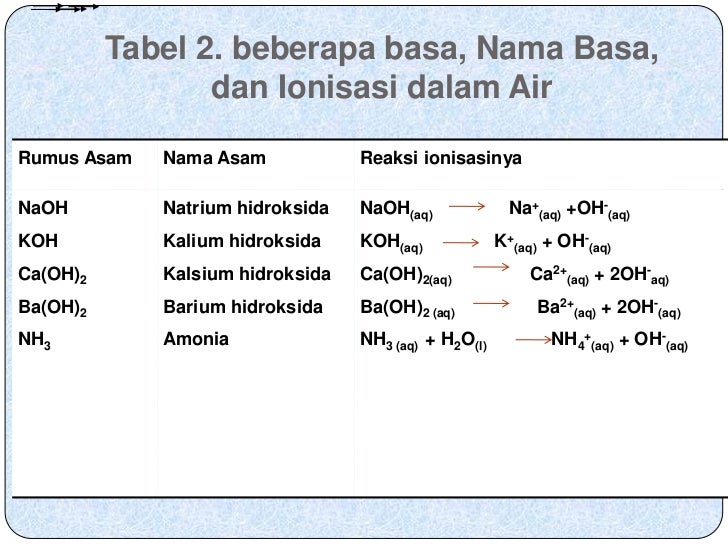
Contoh Asam Basa Kuat Dan Lemah Serta Reaksi Ionisasinya Berbagai Contoh
Mengapa Asam Hidrofluorat Adalah Asam Lemah. Asam fluorida adalah satu-satunya asam hidrohalat (seperti HCl, HI) yang bukan asam kuat. HF terionisasi dalam larutan berair seperti asam lainnya: HF + H 2 O H 3 O + + F -. Hidrogen fluorida sebenarnya larut cukup bebas dalam air, tetapi ion H 3 O + dan F - sangat tertarik satu sama lain dan.

H2S Asam Atau Basa
Asam sulfida (H2S) 21. Asam fosfit (H3PO3) 22. Asam fosfat (H3PO4) 23. Asam arsenit (H3AsO3). Untuk sederhananya di SMA biasanya disebutkan apabila mempunyai Ka atau Kb berarti itu asam atau basa lemah.. nanti langsung akan ketahuan pH nya berapa. kalau pH 1 atau mendekati berarti asam kuat, kalau pH 14 atau mendekati berarti basa kuat. salam

Detail Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Koleksi Nomer 34
Indikator yaitu suatu bahan yang dapat bereaksi dengan asam, basa, atau garam sehingga akan menimbulkan perubahan warna.. Daftar Nama Asam-Basa Kuat & Lemah Asam Kuat : 1. Asam klorida (HCl) 2. Asam nitrat (HNO3) 3.. Asam sulfit (H2SO3) 20. Asam sulfida (H2S) 21. Asam fosfit (H3PO3) 22. Asam fosfat (H3PO4) 23. Asam arsenit (H3AsO3) 24.

Contoh Soal Hidrolisis Asam Lemah Dan Basa Lemah
Tabel Nilai Ka Umum untuk Asam Lemah. K a adalah tetapan kesetimbangan untuk reaksi disosiasi asam lemah . Asam lemah adalah asam yang hanya terdisosiasi sebagian dalam air atau larutan berair. Nilai K a digunakan untuk menghitung pH asam lemah . Nilai pKa digunakan untuk memilih buffer saat dibutuhkan. Memilih asam atau basa di mana pKa.
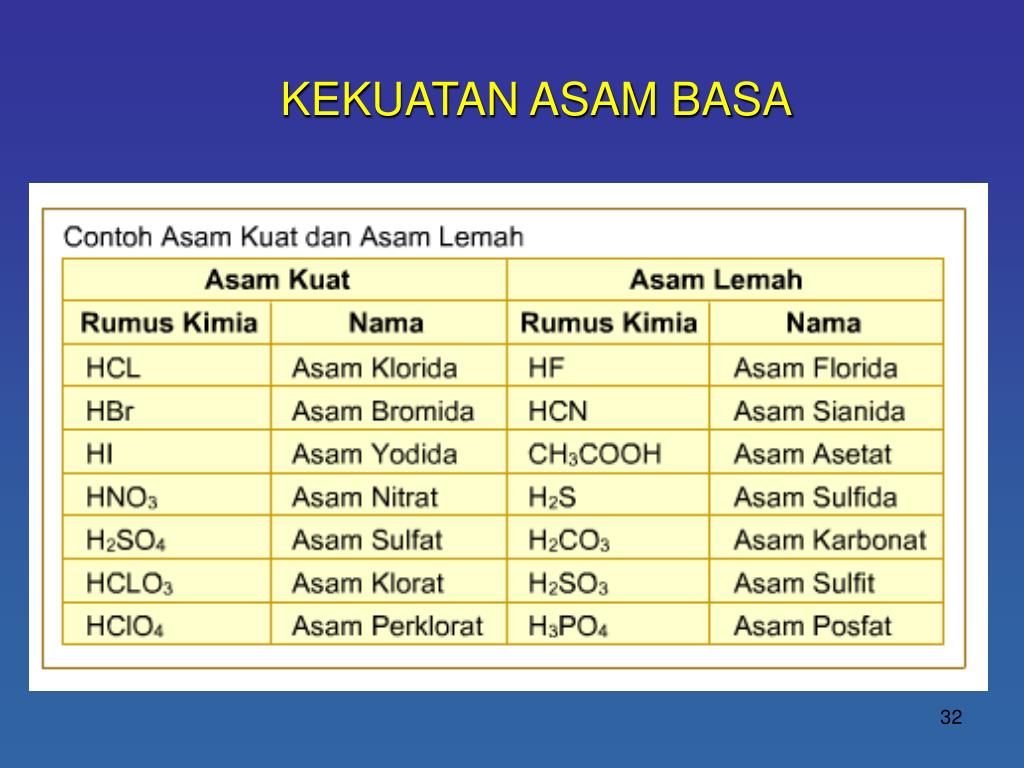
Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Berbagai Contoh
Daftar Nama Asam-Basa Kuat & Lemah. Asam dan Basa memiliki tingkat kekuatan yang berbeda beda. tingkat keasaaman dapat diukur dengan pH. secara umum pH memiliki range dari 1 - 14. semakin rendah pH maka asam akan semakin kuat dan semakin tinggi pH maka tingkat keasaman akan semakin rendah (semakin basa). pH bisa diukur menggunakan Indikator.

20+ Contoh Soal Hidrolisis Asam Lemah Dan Basa Kuat Contoh Soal Terbaru
1. Asam asam merupakan salah satu penyusun dari berbagai bahan makanan dan minuman, misalnya cuka, keju, dan buah-buahan. Menurut Arrhenius, asam adalah zat yang dalam air akan melepaskan ion H+. Jadi, pembawa sifat asam adalah ion H+ (ion hidrogen), sehingga rumus kimia asam selalu mengandung atom hidrogen. Ion adalah atom atau sekelompok atom.

Contoh Asam Basa Kuat Dan Lemah Serta Reaksi Ionisasinya Berbagai Contoh
Air Liquide officially opened its largest liquid hydrogen production and logistics infrastructure facility in North Las Vegas, Nevada. The facility aims to supply the growing needs for hydrogen mobility, but will also allow to provide hydrogen to a wide array of industries while the mobility market continues to mature.
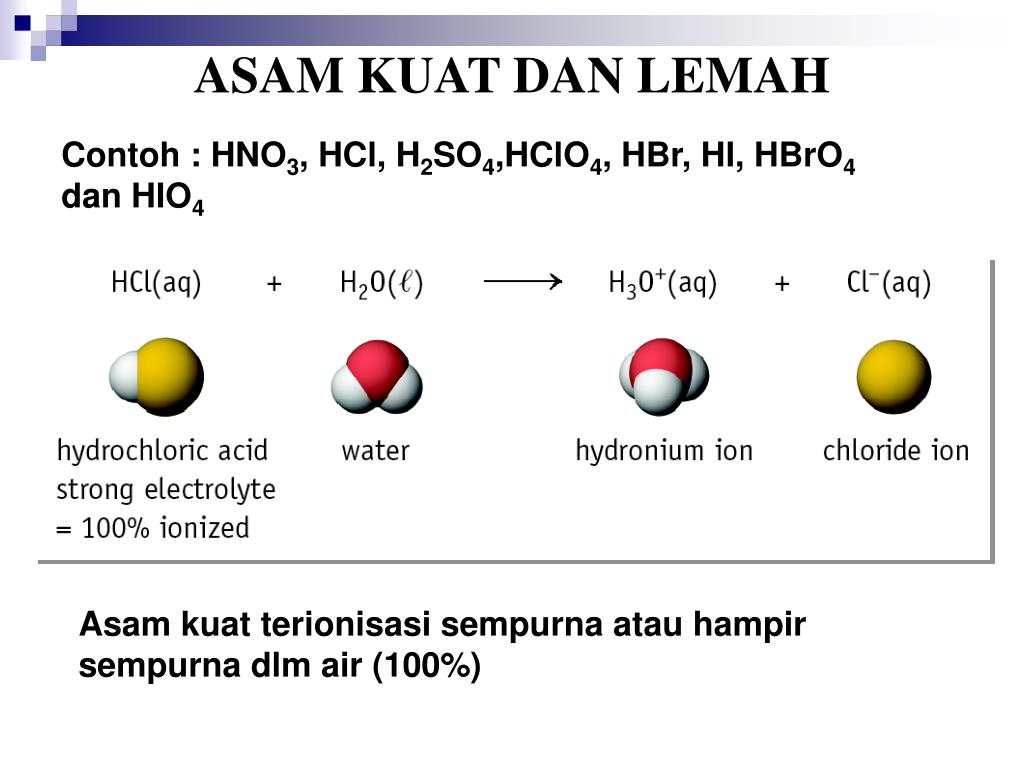
PPT ASAM DAN BASA PowerPoint Presentation, free download ID1244635
Hidrogen sulfida, H 2 S, adalah gas yang tidak berwarna, beracun, mudah terbakar dan berbau seperti telur busuk. Gas ini dapat timbul dari aktivitas biologis ketika bakteri mengurai bahan organik dalam keadaan tanpa oksigen ( aktivitas anaerobik ), seperti di rawa, dan saluran pembuangan kotoran. Gas ini juga muncul pada gas yang timbul dari.

Detail Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Koleksi Nomer 21
Cara membedakan asam kuat dan asam lemah. Nilai konstanta kesetimbangan reaksi disosiasi menunjukkan apakah suatu asam kuat atau lemah . Artinya, konstanta disosiasi asam K a , adalah konstanta kesetimbangan reaksi disosiasi asam dalam media berair (parameter logaritmik juga digunakan, pK a =-logK a ). Nilai K a besar untuk asam kuat (dan pK a.